文献解读|J Hepatol(33):人类肝星状细胞的多模态分析确定了代谢功能障碍相关脂肪变性肝病的新治疗靶点
✦ +
+
论文ID
原名:Multi-modal analysis of human hepatic stellate cells identifies novel therapeutic targets for metabolic dysfunction-associated steatotic liver disease
译名:人类肝星状细胞的多模态分析确定了代谢功能障碍相关脂肪变性肝病的新治疗靶点
期刊:Journal of Hepatology
影响因子:33
发表时间:2025.05.05
DOI号:10.1016/j.jhep.2024.10.044
背 景
代谢功能障碍相关脂肪变性肝病是一系列肝脏疾病,从脂肪变性(代谢功能障碍相关脂肪变性肝 [MASL])到伴有纤维化的代谢功能障碍相关脂肪性肝炎 (MASH)。MASH的诱因包括肝细胞慢性毒性损伤、炎症和纤维化细胞因子(IL-6、TNFα、IL-1β 和 TGFβ1)的上调,以及肝星状细胞(HSC)分化为活化HSC (aHSC)/肌成纤维细胞,进而产生细胞外基质 (ECM)。HSC具有独特的可塑性。在健康肝脏中,静止期 HSC (qHSC) 位于窦周隙,储存维生素 A,并表达神经和脂肪生成(Lrat、Ngfr和Pparg)标志物。在毒性肝损伤反应中,qHSC 转分化为表达Col1a1、Acta2、Timp1、Loxl1的 aHSC/肌成纤维细胞,并产生纤维瘢痕。肝纤维化消退后,aHSC失活,下调纤维化基因的表达,并重新表达一些(Pparg、Apoe和Bambi)但不是全部(Gfap或Adipor1)静止相关基因。此外,在 MASH 小鼠中已研究了炎症 HSC 表型 (INF)。目前尚无针对肝病的抗纤维化疗法。本研究旨在鉴定在人类aHSC中在MASH纤维化发病机制中起关键作用的基因及其调控机制。
实验设计
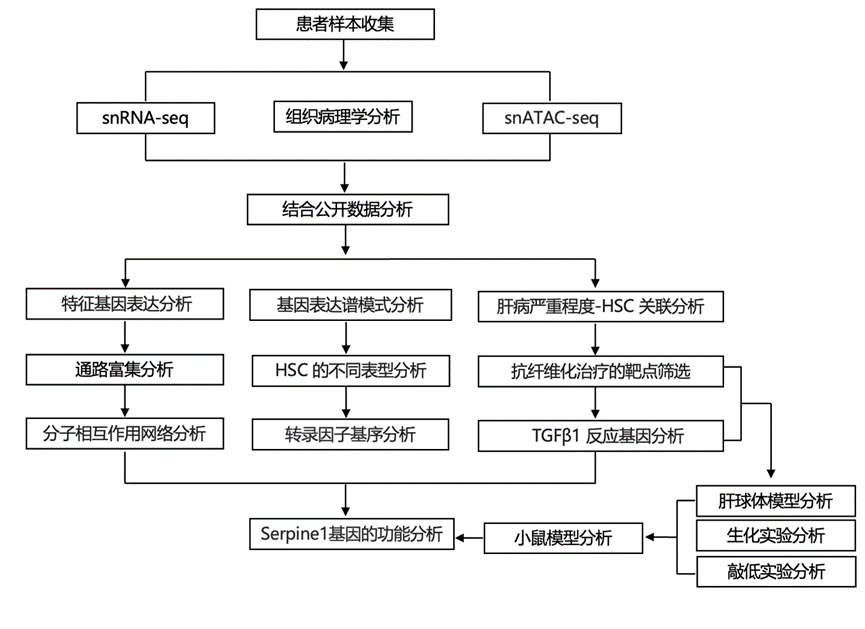
结 果
01
人类正常肝脏、MASL肝脏和MASH肝脏的表征
MASH/临床研究网络评分标准<3诊断为正常肝脏,脂肪变性的肝脏确定为MASL,而评分≥5(伴有脂肪变性、炎症和纤维化)的肝脏则诊断为MASH。本研究涉及的肝脏诊断为正常(n= 5)、MASL(n=4)、MASH(n=9,纤维化2-4期)是通过结合病史和肝组织学来定义的。为了研究MASH肝纤维化的发病机制,研究团队从速冻肝脏中分离了细胞核,并进行了单细胞核转座酶可及染色质测序(snATAC-seq)和单细胞核转录组分析(snRNA-seq)(图1A)。
对 NORMAL、MASL 和 MASH 肝脏数据集进行了整合和聚类。snRNA-seq 和 snATAC-seq数据中的肝细胞类型使用来自 Panglao 数据库的标记以及以下已知标记基因进行注释:HNF4A +(肝细胞)、NGFR+(HSC)、Myh11+(间皮细胞)、PECAM1+(内皮细胞)、CD69+(T 细胞)、CD19+(B 细胞)、CD163+(髓系细胞)和KRT19+(胆管细胞)(图1B-C)。静止和活化标记——CYGB、COL1A1、RBP1和HGF以及NGFR基因——均用于鉴定HSC 群体(图1B-C)。在MASH肝脏中,HSC共表达COL1A2和TIMP1。HSC在正常和MASL肝脏中均有表达(分别占肝细胞总数的4-5%和5-8%),但在MASH肝脏中则扩增至13-20%(图1D-G)。样本平均基因表达的主成分分析显示,MASH HSC与正常和MASL HSC存在显著差异(图1H),这表明MASH HSC的转录差异最大,而正常和MASL HSC的基因表达模式相似。
将每种条件下差异表达的 HSC 基因的差异倍数关联起来表明,MASH HSC 与 NORMAL 和 MASL HSC 有显著差异(图1I-J)。MASH HSC 下调静止相关基因(LRAT、SYNM、SYP)并上调纤维化基因(COL1A2、LOX和TIMP1)。
通路分析显示, MASH HSC 在 ECM 通路中高度富集,而 NORMAL HSC 与维生素 A 的反应和神经元相关发育有关(图 1 K)。同样,MASH 和 NORMAL HSC 表现出不同的染色质可及性模式(图1L-M)。虽然 MASL 和 NORMAL HSC 的基因表达模式主要重叠(图 1 J-M),但 MASL HSC 具有一些独特的特征,例如调节蛋白质和板状伪足组织途径,从而驱动 HSC 运动性(图 1 N),这表明肝脏脂肪变性本身就可以影响 HSC 表型。

图1. 人类NORMAL、MASL和MASH HSC的跨平台表征。
(A) 样本量、数据类型、各平台各条件下的细胞数量。(B) 热图:snRNA-seq 中不同细胞类型的平均相对标记基因表达。(C) snATAC-seq 中细胞类型标记基因的开放染色质区域。(D) UMAP 图显示已鉴定的细胞类型。(E) 组成图和表格显示各条件下的细胞分布。(F) UMAP 图显示已鉴定的细胞类型。(G) 组成图和表格显示各条件下的细胞分布。(H) 各条件下HSC的主成分分析。(I) 相对表达量,可区分正常 (NORMAL)、MASL 和 MASH 型HSC。(J) 不同条件下HSC中差异基因表达的相关性。(K) 最能区分 NORMAL、MASL 和 MASH HSC 基因表达的通路。(L) 相对可及性区分 NORMAL、MASL 和 MASH HSC。(M) 不同条件下 HSC 中差异可及性峰之间的相关性。(N) 最能区分 NORMAL、MASL 和 MASH 肝脏中染色质可及性的选定通路。
02
分子相互作用网络识别出特定条件下的HSC“特征基因”
为了进一步了解共同调控基因的功能,基于STRING数据库中已知的这些基因之间的相互作用,他们构建了NORMAL、MASL和MASH HSC的分子相互作用网络,这些网络包含转录上调和与启动子或增强子区域染色质可及性相关的基因(图2 A-C)。在各状态中同时满足转录上调与表观遗传可及性开放的基因定义为HSC“特征基因”。
正常HSC互作网络包含36个特征基因,其中涉及静息态相关基因(LRAT、MBOAT2、SYT1、COLEC10、CAV2、ERCC10)(图2A)。MASL-HSC网络中特异性诱导了10个特征基因(含静息态相关基因VIPR1、LRAT、NFKBIA)(图2B)。值得注意的是,MASL-HSC中同时满足转录上调与表观可及性的基因重叠度显著低于MASH或正常组,提示表观遗传改变可能先于转录激活发生。MASH-HSC网络包含71个诱导型特征基因,与正常或MASL网络重叠有限,该网络显著富集了纤维化反应和ECM重构相关基因(包含SERPINE1、THBS2、EFEMP1、FBLN5、LAMC3、LAMA2、PRELP、COL4A1及COL1A2)(图2C-E)。
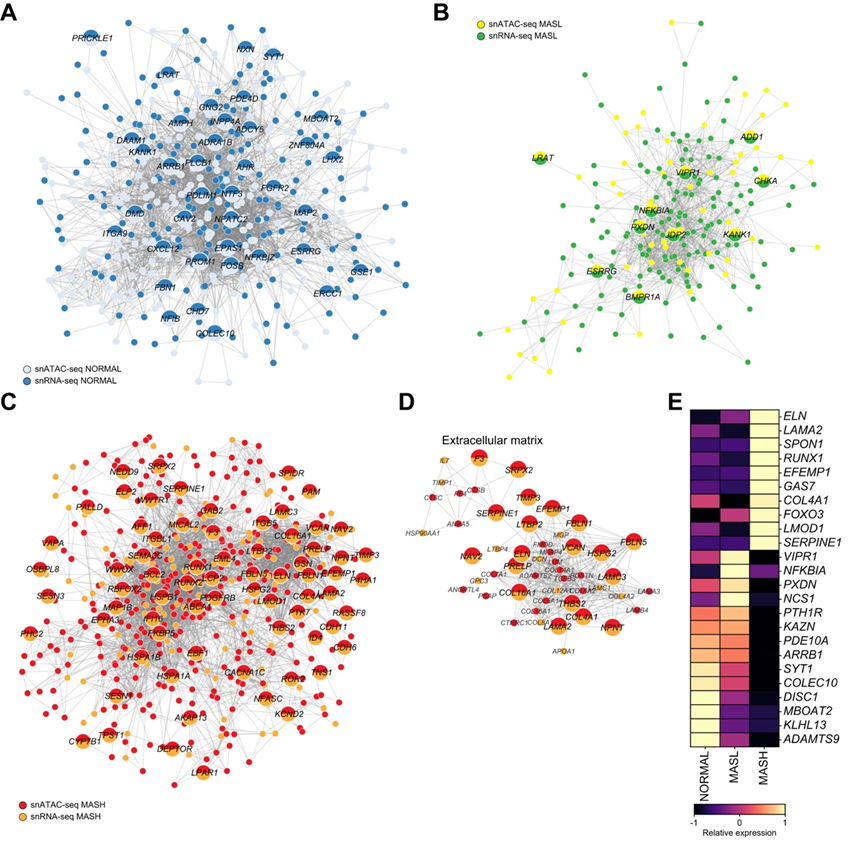
图2. 通过分子相互作用网络整合测序模式。
(A-C) NORMAL、MASL 和MASH HSC 中的分子相互作用网络。(D) MASH HSC 中ECM 组织子网络。(E) 热图:特定于 NORMAL、MASL 和 MASH HSC 的选定基因的相对表达。
03
HSC 表型因情况而异
为解析正常、MASL及MASH状态下HSC的异质性(图3A-D),他们采用小鼠MASH模型鉴定的标志基因集对HSC进行亚群分析(图3E)。基于标志基因保守性,人类HSC亚群与小鼠模型高度吻合。通过多组学测序,在所有状态中均检测到静息态(Q/q)、活化态(A/a)和炎症型(INF)HSC亚群,仅通过snRNA-seq额外识别出两个活化亚群(A1、A2)(图3A-D)。具体而言,NORMAL 和 MASL HSC 主要由LRAT + SYNM + NGFR + QHSC 和少量 AHSC组成。相比之下,MASH HSC 中含有极少量的 QHSC,但富含COL1A2+ LOX + SPP1 + TIMP1 + aHSC,尤其是 A2 亚群(图 3 A-D)。INF占CD36+ CLEC + CREM + HSC的一小部分(4.9%) ,并且在所有条件下均有发现,这表明 Q、A 和 INF 聚类的 HSC 存在于每个人的肝脏中。
值得注意的是,不仅 HSC 组成因条件而异,而且 Q 和 A 聚类的基因表达谱在 NORMAL、MASL 或 MASH HSC 之间也发生变化(图 3 I),这意味着 HSC 群体是异质性的。例如,KALRN、SERPINE1、LAMA2、EFEMP1和ITGB5的表达将 MASH aHSC 与 MASL 或 NORMAL aHSC 区分开来(图3I)。MASL QHSC 和 aHSC 独特地上调了CPXM2、APOE、IGFBP5、ORM1基因的表达(图3I),这些新发现可能鉴定出 MASL 进展为 MASH 的潜在生物标志物。
为了研究 HSC 调控机制,他们首先确定了在每个 HSC 亚群中特异性富集的 snATAC-seq候选顺式调控元件 (cCRE),然后进行了 TF 基序富集分析(图 3 J-K)。亚群特异性 cCRE 的绝对富集鉴定出约 19 个 TF 基序,这些基序在所有 HSC 聚类中均高度诱导(图 3 J)。其中一些 TF与活化相关(JUNB、AP-1、RUNX1、TEAD、SMAD、STAT、MEF),而其他(ETS、IRF、GATA)则与谱系决定和静止 HSC 表型的维持有关。谱系决定 TF 在特定细胞类型中含量丰富,以细胞特异性方式结合增强子,它们的缺失可能导致细胞命运发生改变。由于这些约 19 种 TF 具有高度且普遍存在的基序富集,因此它们可能属于谱系决定 TF 的类别(图 3 J),这表明差异可及的谱系决定 TF 可调节 HSC 表型。
TF基序的相对富集揭示了每个谱系决定TF在聚类富集的cCRE中优先富集(图3K)。例如,与激活相关的JUNB/AP1基序在与A聚类相关的cCRE(图3K)、ETS1和IRF1/2在Q聚类相关的cCRE中显著富集,而与INF聚类相关的cCRE则在MEF2和NFY中富集。
此外,仅在来自特定 HSC 聚类的 cCRE 中观察到所选聚类特异性 TF 和谱系决定 TF 高度富集之间的强相关性(图 3 J-K)。聚类特异性 TF 定义为仅在功能不同的 HSC 亚群中上调的一组 TF。他们假设聚类特异性 TF 可能决定每个细胞亚群的表型。例如, RUNX1/2在与 A 相关的 cCRE 中富集程度最高,Lhx1/2和FXR与 Q 相关的 cCRE 中富集程度最高,EBF与 INF 相关的 cCRE 中富集程度最高(图 3 J-K)。由于聚类特异性 TF 的结合位点通常位于 HSC 谱系决定 TF 的 cCRE 内,聚类特异性TF 可能调节谱系决定 TF 的转录。对启动子连接的cCRE(CICERO)中检测到的基序的分析表明,谱系特异性IRF1可由RUNX1/2和FXR共同调控,而JUNB和GATA6可能通过ETS1/2-RUNX1/2之间的相互作用共同调控。总体而言,不同的聚类决定TF和谱系决定TF组合可产生多种信号来控制HSC表型以响应疾病。
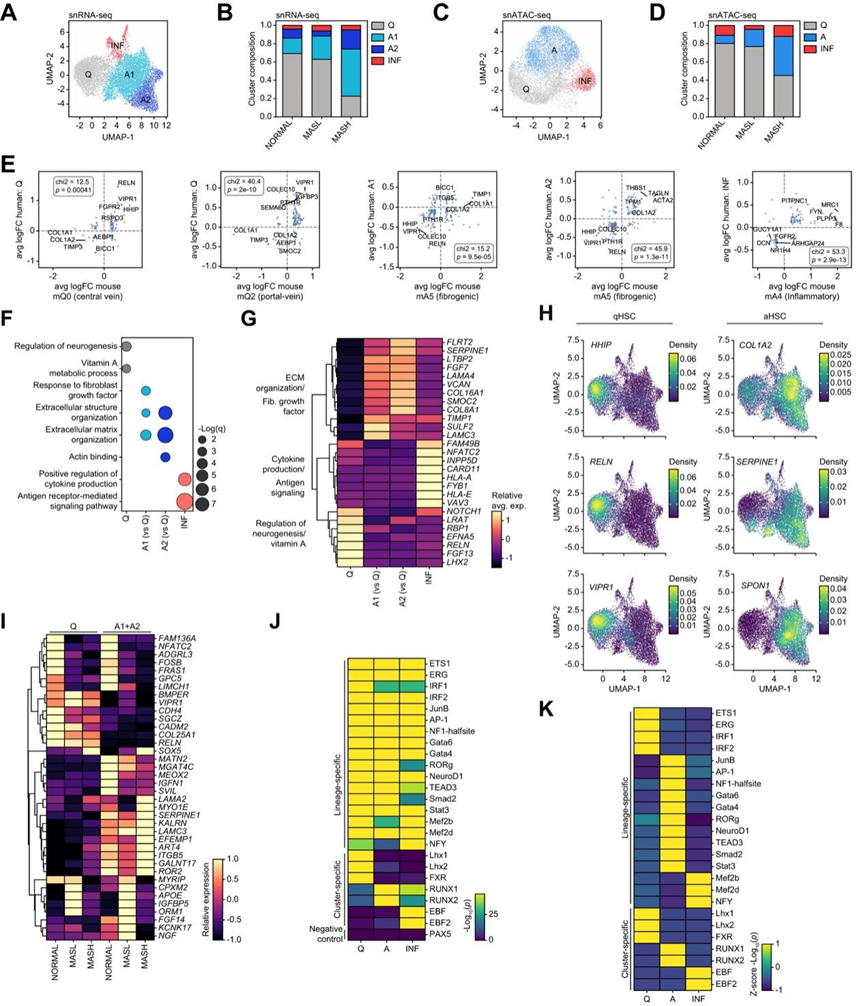
图3. NORMAL、MASL 和 MASH HSC 的亚群。
(A-D) UMAP 降维图和描述不同条件下亚聚类的组合图。(E) 散点图显示小鼠和人类 HSC 亚聚类之间“标记基因”的重叠表达。(F) 区分每个 HSC 亚聚类的代表性通路。(G) 特异性通路基因的相对表达。(H) UMAP 密度图显示选定的静止和激活基因的表达。(I) 选定基因相对表达的热图。(J-K) 热图中显示了差异可及峰/聚类的绝对和相对基序富集和结合转录因子。
04
HSC 活化与肝纤维化的严重程度相关
结合snRNA-seq 数据比较不同供体的 HSC 聚类组成时,发现其与肝纤维化阶段直接相关(图 4 A-C)。NORMAL 和 MASL 供体在 Q 聚类中的细胞比例最高。正如预期的那样,患有重度纤维化(4 期)的 MASH 供体在纤维化 A1 和 A2 聚类中的细胞比例最高,而在 Q 聚类中的细胞相对较少(图 4 A-B)。2-3 期纤维化的 MASH 供体在 A1 和 Q 聚类中拥有 HSC 的可能性高于在 A2 聚类中拥有 HSC 的可能性(图4B-C)。使用 Slingshot进行的伪时间轨迹分析确定了 HSC 分化的单一路径,该路径始于 Q 聚类并通过 A1 向 A2 发展(图 4 D-E),这表明静止的 HSC 逐渐激活为 A1 和 A2 HSC。沿伪时间路径,激活特异性基因(SERPINE1、EFEMP1、ACTA2、COL1A2)的表达在A1至A2聚类中上调,而典型的静止标记(RELN、VIPR1、RBP1)的表达下调(图4F)。
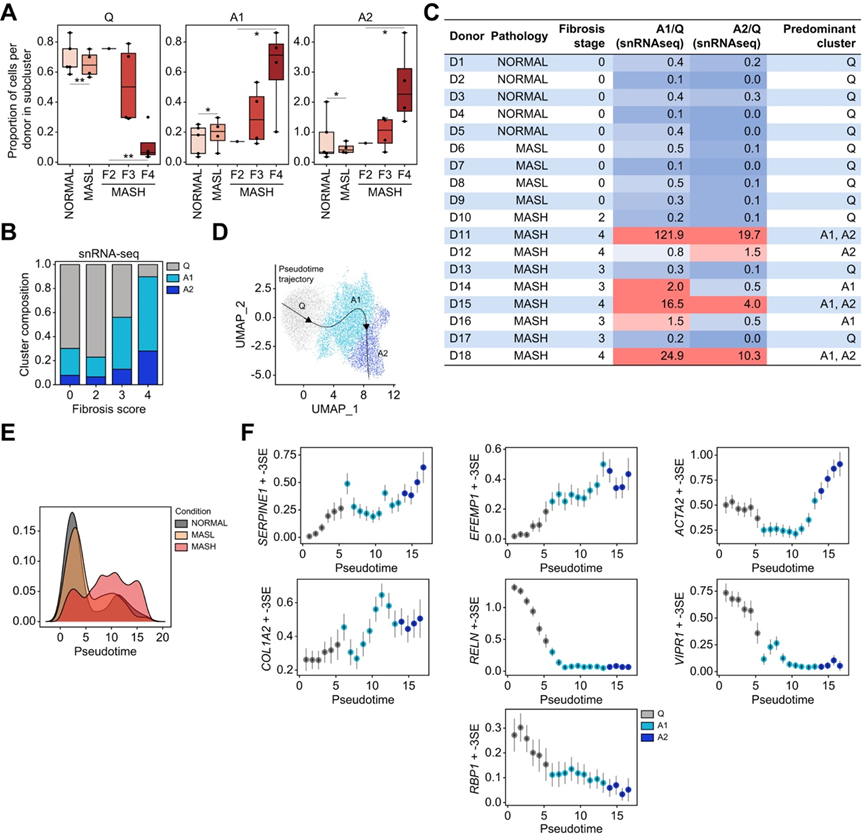
图4. MASH HSC 的 Q、A1 和 A2 亚聚类的独特特征。
(A) 亚群组成分布揭示了正常、MASL 和 MASH HSC 的群异质性。(B) 堆叠条形图显示 Q、A1 和 A2 HSC 按纤维化评分的组成。(C) A1 主要与 3 期纤维化一致(供体 D14、D16);A2 主要与 4 期纤维化一致(D12)。三名供体的细胞在 A1 和 A2 之间均匀分布(D11、D15 和 D18,纤维化为 4 期)。(D) 伪时间轨迹映射到 HSC UMAP 坐标。(E) 不同条件下 HSC 沿伪时间坐标的分布。(F) HSC 标记基因的平均表达沿分箱伪时间绘制。
05
抗纤维化治疗新靶点的优先排序
他们推测潜在的抗纤维化治疗靶点会在MASH模型及活化HSC中呈现上调表达且染色质可及性增加。为验证该假说,他们筛选了同时满足以下条件的基因:(1)在MASH与NORMAL+MASL的HSC间存在差异表达及染色质可及性变化;(2)在aHSC与qHSC间存在相同趋势变化。最终鉴定出146个在MASH aHSC中可及性增强且表达上调的基因,其中13个基因属于肌动蛋白丝组织通路,23个基因属于ECM通路——这与前期发现的ECM通路在MASH HSC中显著富集的结果一致(图5A)。基于这些基因在生物学相关通路中的参与度,他们选择6个基因进行实验验证:SERPINE1、GAS7、EFEMP1、SPON1、KLF9和LTBP2(图5A-D)。
使用 CICERO 评估所选六个核心基因的潜在顺式调控关系。例如,在SERPINE1基因位点中,鉴定出SERPINE1和邻近TRIM56的假定增强子-启动子元件之间存在共可及的峰/cCRE(以连接线显示)(图 5 E),这表明这些基因可能受到共调控。SERPINE1基因上游和下游可及染色质区域高度富集JUNB/AP1、RUNX1/2(激活相关转录因子)和ETS1(最有可能抑制SERPINE1表达)等基序。一致地,在小鼠 aHSC 中体外敲低ETS1/2导致SERPINE1、LTBP2、GAS7、EFEMP1和 SPON1 基因强烈上调,表明这些基因可能由共同的信号通路激活。他们分析了 TF-靶基因关系数据库,SERPINE1、LTBP2、GAS7、EFEMP1、SPON1 和KLF9(蓝色圆圈)由一小组TF (红色三角形)共同调控,其中包括FOX、RUNX、SREBP1、ELF3、FOXA1、HOXA13等(图 5 F)。其中一些 TF 参与调节 TGFβ1 介导的纤维化反应,属于“信号依赖性” TF。这些因子各自调控多个MASH活化HSC特异性靶基因,并与聚类特异性及谱系特异性转录因子形成互作网络。通过FIMO(特定基序识别)进行的基序富集分析展示了转录因子与目标基因的相互作用(图5G)。RUNX1/2在整个分析中鉴定为谱系、聚类及ECM特异性转录因子的潜在共激活因子(图5G),提示其可能作为纤维化反应的主调控因子。他们推测TGFβ1响应的FOXP1和FOXA1/2可激活RUNX1/2,进而诱导JUNB/AP-1转录超过基础水平,最终抑制ETS1/2(图5H)。为验证此假说,在MASH患者来源的人HSC(供体D23)中,RUNX1/RUNX2的dsiRNA敲低可抑制TGFβ1诱导的纤维化激活及SERPINE1表达。通过电泳迁移率变动分析和位点特异性染色质免疫沉淀证实,RUNX1/2能直接结合SERPINE1增强子cCRE并驱动其转录,表明阻断HSC中RUNX1/2-SERPINE1相关通路可减轻肝纤维化(图5I-J)。RUNX1/2与其他核心基因的相互作用通过FIMO 基序富集得到验证。
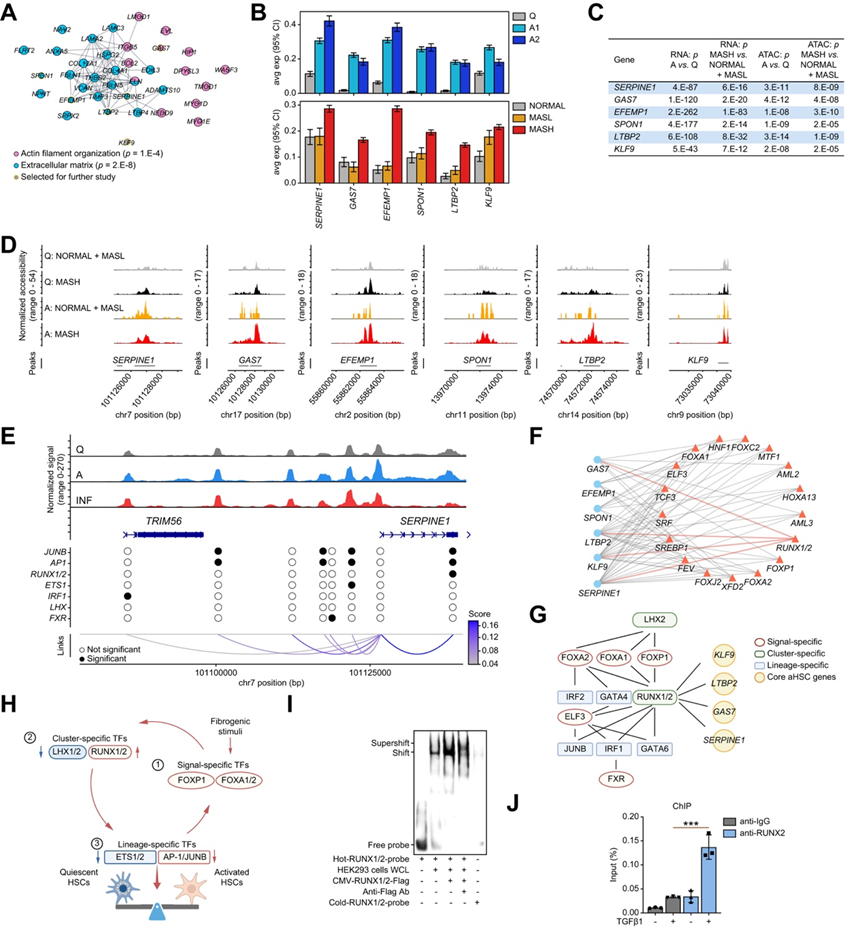
图5. 介导MASH HSC中ECM组织网络的基因。
(A) 在 MASH aHSC 中可及性和上调的基因网络。(B) 选定的六个核心 MASH aHSC 的基因按聚类和条件的平均表达。(C) 差异表达/可及性统计数据。(D) 标准化的可及性峰值。(E) SERPINE1 周围区域的可及性图。(F) 已知靶向 ≥2 个 aHSC 基因的 TF 网络。(G) 根据信号、聚类和谱系特异性 TF 与选定的核心 aHSC 基因之间的预测调控关系构建的网络。(H) 通过 TF 之间的相互作用调控 HSC 活化。(I) EMSA 证明CMV- RUNX1/2- Flag 转染的 HEK293裂解物的RUNX1与Serpine1增强子探针有特异性结合。(J) RUNX2基因座特异性 ChIP 分析。
06
GAS7、SERPINE1、SPON1、LTBP2鉴定为 HSC 中的 TGFβ1 反应基因
使用来自患有 MASL 和 MASH 的患者培养的人类 HSC,进一步在体外评估了六个核心 MASH 特异性纤维化 HSC 基因SERPINE、LTBP2、GAS7、EFEMP1、SPON1和KLF9的功能特性。在 TGFβ1(5 ng/ml)刺激的人类 HSC 中,GAS7、SERPINE1、SPON1、LTBP2(但不是 EFEMP1 或 KLF9)的表达上调(图6 A),表明这些基因对TGFβ1有反应。使用 dsiRNA 敲低进一步评估了GAS7、SERPINE1、SPON1和LTBP2基因在 HSC 活化中的作用。在转染了基因靶向 dsiRNA 的 HSC 中,基因敲低率超过 85%(图 6 B-C)。结果显示,敲低SERPINE1、GAS7、SPON1或LTBP2均能显著抑制TGFβ1刺激的人HSC中促纤维化基因的表达。值得注意的是,SERPINE1敲除还下调了GAS7、SPON1和LTBP2的表达,提示SERPINE1在HSC活化中起关键作用。此外,在人原代HSC中敲低GAS7、SPON1或LTBP2也能抑制SERPINE1的诱导表达(图6C),表明这些基因可能存在协同调控关系。
通过共培养肝脏所有细胞类型(肝细胞、非实质细胞及肝星状细胞,比例模拟肝脏原位组成)构建人源肝脏球体模型,并使用MASH诱导剂刺激7天。在MASH肝脏球体中检测到肝毒性损伤标志物(G6PC和CYP2E1)、脂滴沉积(BODIPY染色)及促纤维化基因(COL1A1和ACTA2)上调,同时活化的Vimentin+αSMA+肝星状细胞/肌成纤维细胞内PAI-1和Spondin1蛋白表达增加,表明该模型能准确模拟人类肝脏对代谢损伤的反应特征(图 6D-E)。
在构建肝脏球体模型前,对HSC进行GAS7、SERPINE1、SPON1和LTBP2的基因敲低。结果显示,特异性敲低HSC中的SERPINE1和SPON1(而非GAS7或LTBP2)可显著抑制MASH球体中COL1A1和ACTA2的mRNA及蛋白表达(图6E-H)。SPON1敲除还降低了MASH球体中HSC的PAI-1表达(图6G)。相反,特异性敲低静止态相关基因RELN会诱导SERPINE1 mRNA表达,并伴随MASH球体中I型胶原和αSMA蛋白的急剧上调(图6I-J)。他们提出SERPINE1表达是HSC活化的关键调控节点。与此一致,采用PAI-1抑制剂TM5441(20或40 μM)进行药理抑制,能以剂量依赖方式降低人HSC(无论是否经TGFβ1刺激)及人MASH肝脏球体中的I型胶原生成,提示SERPINE1可作为抗纤维化治疗的潜在靶点。
在TGFβ1刺激的HSC中敲低SERPINE1导致GAS7、SPON1和LTBP2表达下调。鉴于这四种基因均受TGFβ1调控(图6A),他们推测SERPINE1敲低的活化HSC中活性TGFβ表达可能受损。实验证实,含SERPINE1敲低HSC的MASH肝脏球体分泌的活性TGFβ1减少50%(相比于对照组),表明SERPINE1表达水平影响TGFβ1活性(图6K)。与此一致,在SERPINE1敲低的肝脏球体中观察到潜伏态TGFβ累积,同时HSC中整合素αv(通过结合潜伏相关肽从复合体中释放活性TGFβ的关键调控因子)表达显著下调(图6L)。为解析PAI-1调控TGFβ激活的机制,他们将SERPINE1敲低或对照HSC经TGFβ1刺激后,与转染TGFβ启动子驱动荧光素酶报告基因的HEK293T细胞共培养以检测活性TGFβ释放(图6M)。结果显示,TGFβ1刺激的HSC强烈诱导HEK293T细胞荧光素酶活性,而SERPINE1敲低显著抑制活性TGFβ生成。这些数据表明,SERPINE1通过整合素αv介导的胞外潜伏态TGFβ激活来调控HSC的TGFβ1应答。HSC中PAI-1缺失导致整合素αv表达下降,维持TGFβ潜伏状态,从而抑制HSC中TGFβ响应基因的表达(图6 N)。
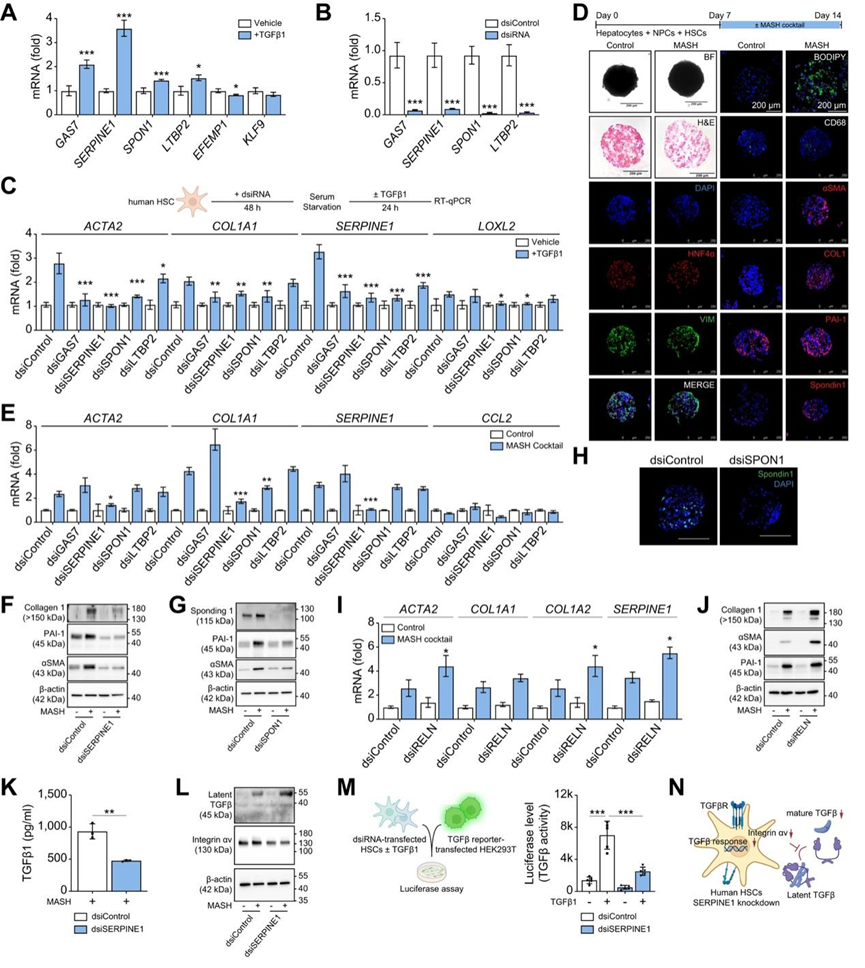
图6. HSC特异性敲低SERPINE1可抑制 MASH 引起的人类肝球体纤维化反应。
(A,C) 通过 qRT-PCR 分析培养的人类 MASL 和 MASH HSC。(B) 用基因靶向dsiRNA 转染 HSC,通过 qRT-PCR 测量基因敲低效率。(D) 免疫染色分析。(E-G) 使用qRT-PCR、免疫印迹法和免疫组织化学法评估对照和含有 dsiRNA 基因靶向 HSC 的 MASH 肝球体中纤维化基因的表达。(I-J) 使用qRT-PCR 和免疫印迹法评估对照和含有RELN敲低的 HSC 的 MASH 肝球体。(K-L) 使用敲低SERPINE1 的HSC ± MASH 混合物生成人肝球体,使用人 TGFβ1 ELISA 分析 MASH 球体上清液中的活性 TGFβ1,对球体裂解物中潜在 TGFβ1 和整合素 αv 表达进行免疫印迹分析。(M) 通过测定荧光素酶活性评估与HSC(供体D23)共培养的HEK293T细胞中TGFβ的激活情况。(N) PAI-1调控HSC表型的潜在机制示意图。
07
Serpine1基因缺失可阻止CCl4诱导的HSC活化
为了研究Serpine1在肝纤维化中的作用,他们将 Lrat Cre小鼠与Serpine1 f/f小鼠杂交。将 HSC Δ Serpine1(HSC 特异性Serpine1敲除小鼠)、杂合 HSC Serpine1f/-和野生型 (WT) Serpine1f/f小鼠用四氯化碳 (CCl4) 处理 2 周(图 7 A-C)或 6 周(图 7 D-F)。从这些小鼠中分离 HSC 并进行分析。与 WT qHSC 相比,在CCl4损伤后,WT aHSC 中Serpine1的表达发生显著上调(图 7 A-D)。如预期的那样,CCl4损伤的 HSC Δ Serpine1小鼠的 aHSC 中Serpine1的表达消失。值得注意的是,在接受CCl4处理 2 周后,HSCSerpine1 f/-小鼠的 aHSC 中Serpine1的表达降低了 70% 以上,在接受CCl4处理 6 周后,Serpine1 的表达下调了 93% 以上(图 7 A-D),这表明,单个Serpine1等位基因的敲除可显著抑制 HSC 活化(图 7 A-F)。
比较了CCl4(6 周)损伤的 WT 小鼠和 HSCΔ Serpine1 小鼠的肝纤维化发展情况(图7 G-L)。基于 snRNA-seq 分析,人类SERPINE1主要在人类 MASH 肝脏中的 HSC 和肝细胞中表达(图 S18B,C)。因此,在 CCl4 -HSCΔ Serpine1 小鼠的整个肝脏中,小鼠 Serpine1 mRNA 的表达降低了50 % 以上,导致血浆分泌型 PAI-1 水平显著降低(图7G-H)。
与野生型小鼠相比,CCl4损伤的 HSC ΔSerpine1小鼠肝脏的肝纤维化发展受到强烈抑制,表现为天狼星红和 αSMA 阳性染色降低,纤维胶原密度降低,以及Col1a1、Col1a2、Col3a1、Acta2、Tgfb1、Timp1和其他纤维化标志物的下调(图7I-L),但没有炎症。此外,在 CCl4 损伤的 HSC Δ Serpine1小鼠中,整合素 αv 蛋白的表达也降低(图7 M)。
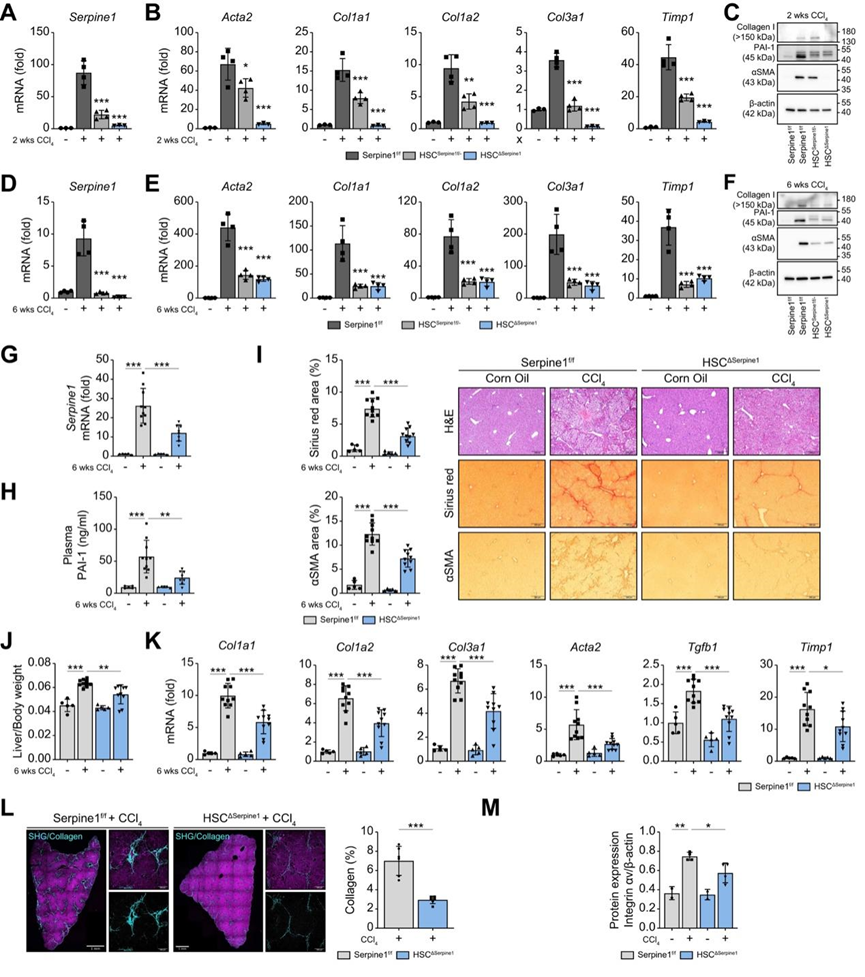
图7. HSC特异性基因敲除Serpine1可抑制CCl4诱发的小鼠肝纤维化。
(A-B)不同基因的相对表达。(C)免疫印迹分析。(D-E)不同基因的相对表达。(F) 免疫印迹分析。(G) 检测肝脏中的Serpine1 mRNA水平。(H) 血浆中的 PAI-1 水平。(I)组织学分析。(J-K) 评估肝重与体重的比率和纤维化基因表达。(L) 肝纤维化的显微观察。(M) 使用免疫印迹法检测肝脏中的整合素 αv 蛋白表达。
08
HSC中Serpine1基因缺失可改善小鼠MASH诱导的肝纤维化
WT 和 HSC ΔSerpine1小鼠以西方饮食(含 30% 果糖水的 AIN-76A 饮食)喂养 24 周以诱导 MASH(图8A)。作为对 MASH 的反应,WT 小鼠的肝脏/体重、肝脏Serpine1和血浆 PAI-I 表达水平显著升高。HSC 特异性敲除Serpine1显著降低肝脏Serpine1和血浆 PAI-1 水平,表明 HSC 贡献了 MASH 小鼠循环 PAI-I 的 50%(图 8 B-C)。此外,患有 MASH 的HSCΔ Serpine1小鼠的肝脏/体重和肝脏脂肪变性降低(图 8 D-F),表明肝脏中Serpine1的水平影响肝脏脂肪生成。HSCΔ Serpine1小鼠免受 MASH 诱导的肝纤维化(与 WT 小鼠相比),如天狼星红、Desmin 和 αSMA 染色减少(图8G-J)以及Col1a1、Col1a2、Col3a1、Acta2、Tgfb1和Timp1基因下调所示(图8K)。
总体而言,针对HSC特异性靶向Serpine1可改善肝纤维化发展。靶向RUNX1/2-SERPINE1轴或可为肝纤维化的治疗提供一种新的策略。
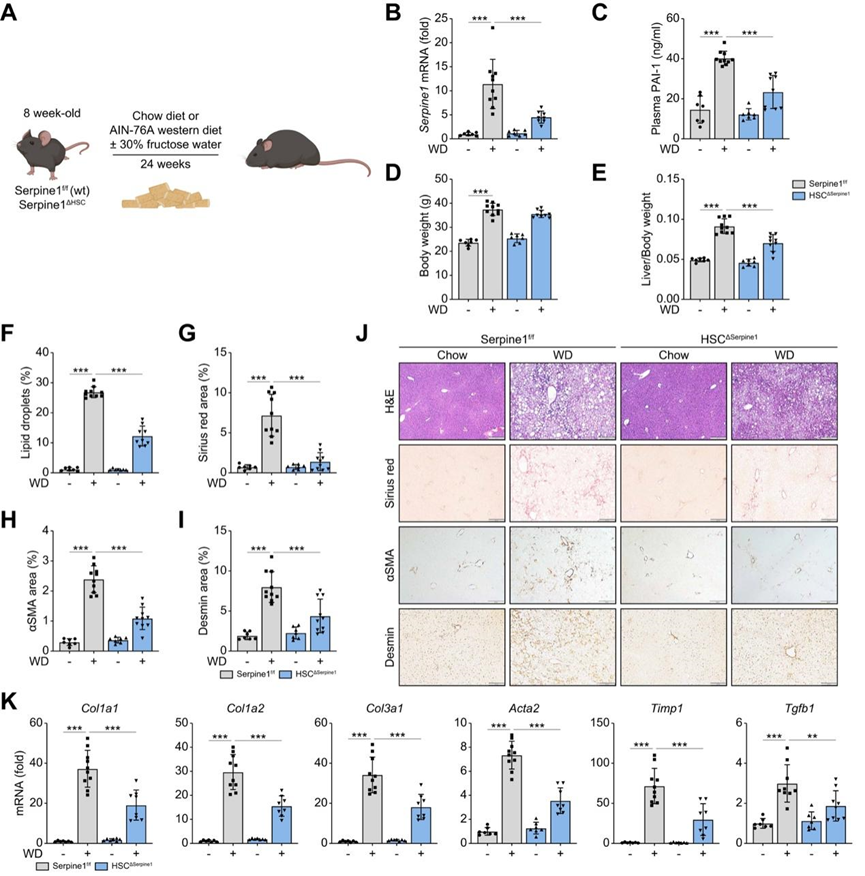
图8. HSC特异性基因缺失Serpine1可抑制小鼠MASH诱导的肝纤维化。
(A) 实验概要:西方饮食诱导的肝纤维化。(B) 检测肝组织中Serpine1 mRNA 的表达。(C) ELISA 检测血浆中 PAI-1 水平。(D-E) 分析体重和肝重与体重的比值。(F-I) WT 和 HSC Δ Serpine1小鼠的肝脏分别用H&E、天狼星红、抗 ɑSMA 和抗 Desmin 抗体染色;阳性面积以百分比计算。(J) 染色肝切片的代表性图像。(K)小鼠肝组织中纤维化基因的表达。
+ + + + + + + + + + +
结 论
本研究介绍了对正常、MASL和MASH患者肝脏中HSC进行多模态测序分析的结果,鉴定了先前研究未检测到的其他亚群,并阐明了 MASH 肝脏中 HSC 的激活机制,包括诱导 HSC 转分化为肌成纤维细胞的转录机制。本研究首次描述了激活的 HSC 衍生的 PAI-1(SERPINE1基因的产物)在 MASH 肝纤维化发展中的致病作用,靶向RUNX1/2-SERPINE1轴可能成为治疗患者肝纤维化的一种新策略。
+ + + + +



 English
English


