文献解读|Cell(42.5):恒河猴屏状体的单细胞空间转录组图谱和全脑连通性
✦ +
+
论文ID
原名:Single-cell spatial transcriptome atlas and whole-brain connectivity of the macaque claustrum
译名:恒河猴屏状体的单细胞空间转录组图谱和全脑连通性
期刊:Cell
影响因子:42.5
发表时间:2025.04.03
DOI号:10.1016/j.cell.2025.02.037.
背 景
屏状体是位于岛叶皮质下方的薄端脑结构,它与几乎所有皮质区域相互连接。大量研究揭示了屏状体对皮质和大脑功能(如睡眠调节、显著性引导注意力、抑郁、行为参与、认知控制和和意识)的作用。早期对恒河猴的解剖学研究表明,屏状体区域及其相应的皮质靶区具有粗略的拓扑结构。单细胞空间转录组学的最新进展阐明了啮齿动物和灵长类动物许多脑区域中不同细胞类型的基因表达情况。然而,灵长类屏状体中细胞类型的空间分布及其全脑连接仍然知之甚少。恒河猴的屏状体明显地由外囊 (ec) 和极囊 (exc) 的白质所划分。小鼠和人类屏状体的单细胞转录组学分析表明,一些屏状体细胞与皮质神经元共有标记基因。然而,恒河猴脑中的屏状体和其它脑区之间的细胞类型的整体相似性尚未检验。一些恒河猴研究表明,屏状体与大脑皮质第 6b 层具有相同的发育起源,但另一些研究表明它起源于一个不同的侧外套膜区域。对屏状体和其它脑区转录组定义的细胞类型进行全面比较可能有助于解决这些问题。
实验设计
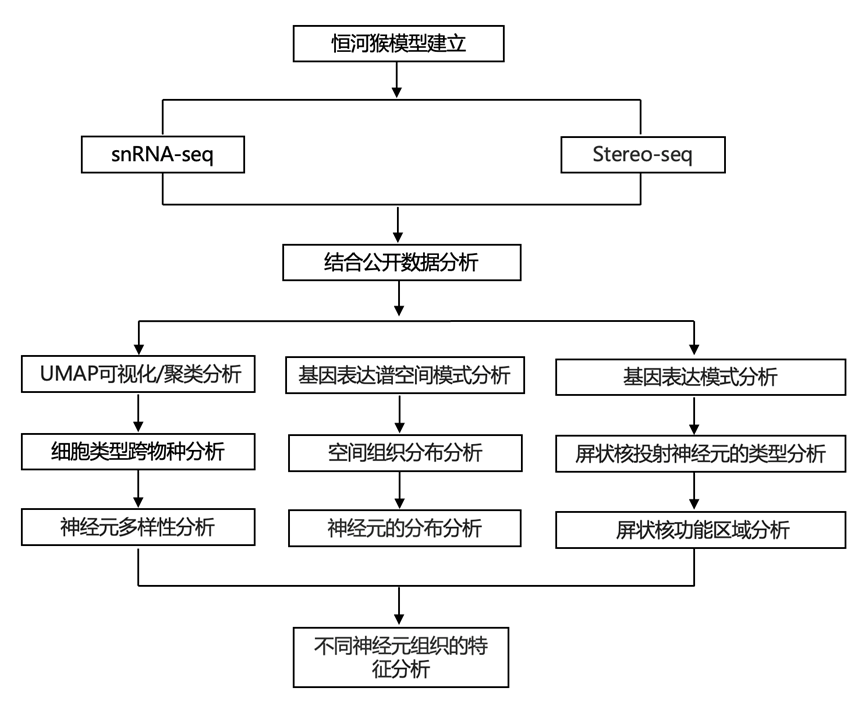
结 果
01
恒河猴屏状体细胞类型的转录组分类
研究团队对四只成年恒河猴的屏状体细胞进行了单细胞核转录组(snRNA-seq)分析,并使用无监督均匀流形近似与投影 (UMAP) 聚类方法,根据基因表达谱的相似性识别可能的细胞类型。他们还对两只恒河猴左半球 67 个屏状体冠状切片进行了单细胞空间转录组分析 (Stereo-seq)。通过将空间图谱中的细胞与 snRNA-seq 定义的细胞类型的基因表达谱进行匹配,对细胞进行了注释(图 1 A)。
经过质量控制后,snRNA-seq 分析纳入 227750 个细胞,平均每个细胞有 4664 个分子标识符(MID)和 1884 个检测到的基因(图 S1 A)。UMAP可视化确定了三大细胞类(“谷氨酸能” [GLUT]:122006 个细胞;“GABA 能” [GABA]:34293 个细胞;“非神经元”:71451 个细胞),进一步分为 16 个亚类(图 1 B),包括 3 个谷氨酸能细胞(以GNB4、RGS6和ZFPM2为标记)、8 个 GABA 能细胞(LAMP5、VIP、RELN、PVALB、SST、PDE10A、LHX6和UNC5B)和 5 个非神经元亚类,包括星形胶质细胞(SLC1A2)、少突胶质细胞前体细胞(OPC、PCDH15)、少突胶质细胞(MOBP)、小胶质细胞(C1QB)和内皮细胞(FLT1)。大多数亚类包含来自所有四只猴子的细胞(图 S1 B),证实了数据的可重复性,并通过随机森林分析进一步验证了这一点(图 S1 C)。16 个亚类可以进一步分为 48 种假定的“细胞类型”:22 种谷氨酸能细胞类型、19 种 GABA 能细胞类型和 7 种非神经元细胞类型(图 1 C,图S1 D)。使用“空间 ID”,他们在两只恒河猴的测序图谱中注释了39 个细胞,将它们与 48 种 snRNA-seq 定义的细胞类型进行匹配。细胞类型分布在猴子之间是一致的(图 S1 E),各种细胞类型的比例与 snRNA-seq 分析发现的比例相似(图 S1 F)。
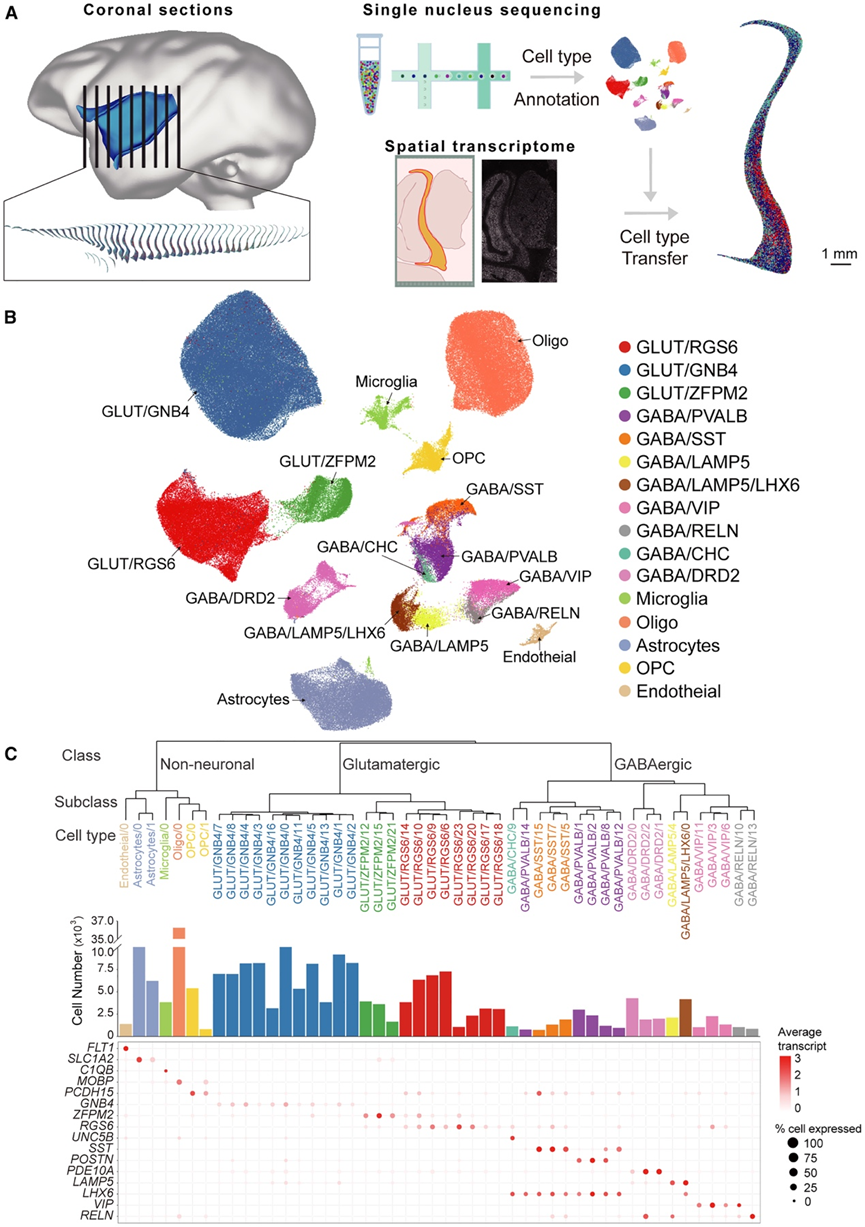
图1. 恒河猴屏状体细胞类型分析。
(A) 实验设计示意图。(B)恒河猴屏状体 snRNA-seq 数据的 UMAP 分析。(C) 上图为细胞分型树状图,显示了恒河猴屏状体的3个主要细胞类、16个亚类和48种细胞类型。
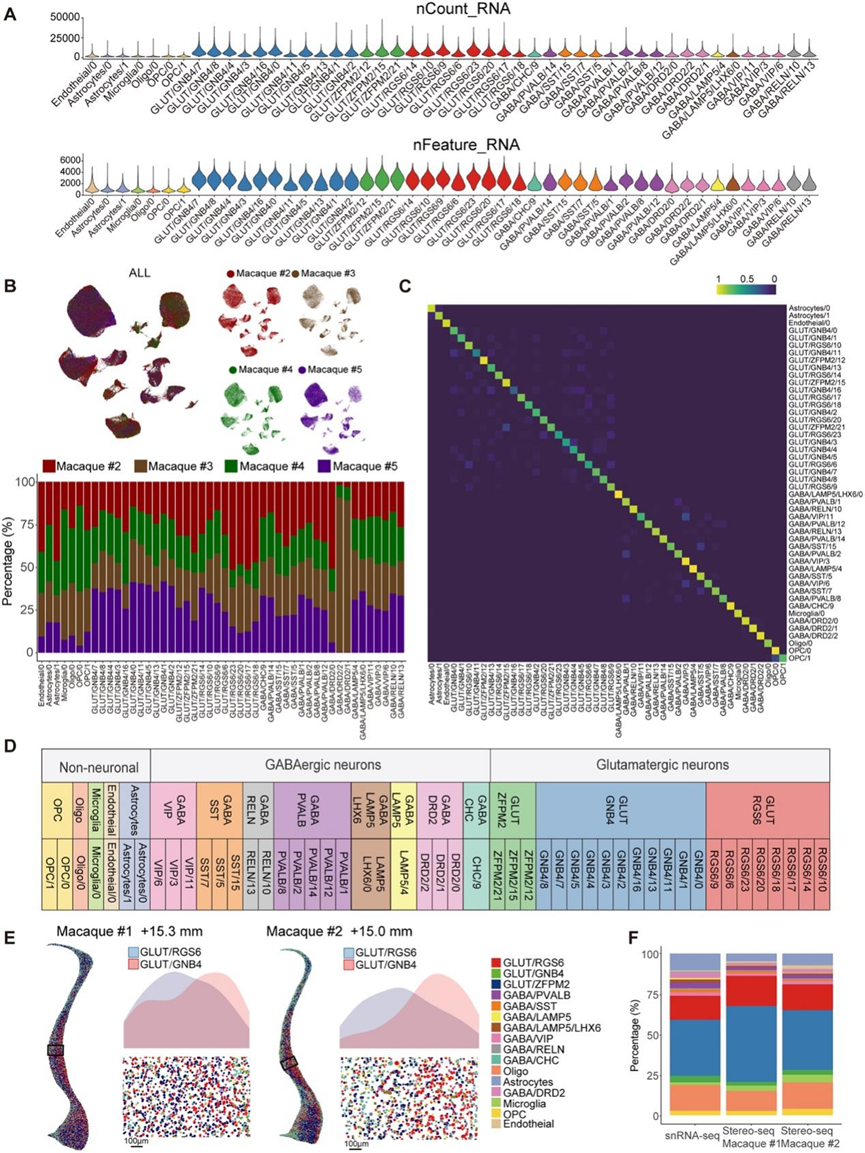
图S1. snRNA-seq和Stereo-seq数据的细胞类型注释。
(A) 小提琴图显示了 48 种细胞类型中每种细胞的唯一分子标识符(nCount_RNA)的丰度和检测到的基因的数量(nFeature_RNA)。(B) 对来自4只恒河猴细胞的snRNA-seq数据进行UMAP聚类分析(左上图),并分别对4只恒河猴的UMAP分布进行分析(右上图)。结果显示,几乎所有的聚类都包含来自所有4只恒河猴的细胞。下方的直方图显示了每只恒河猴的细胞占每种细胞类型细胞总数的百分比(下图),表明聚类分析中的样本偏差较小。(C) 热图显示了应用于来自 snRNA-seq 数据的 48 个细胞聚类的随机森林分类器的混淆矩阵,显示了细胞聚类的可靠性。(D) 表格更清晰地展示了细胞类型分类的层级结构:3个主要类别、16个亚类和48种细胞类型。(E) 左图:所有16个亚类的细胞以点状显示,并以颜色编码。右下图:每张切片中选定区域(黑框)内所有细胞亚类的放大空间图。右上图:每张切片中选定区域(黑框)内GLUT/GNB4和GLUT/RGS6亚类的密度分布曲线。(F) snRNA-seq 数据和Stereo-seq 数据中所有细胞中来自不同亚类的细胞的百分比,显示不同亚类中细胞的百分比大致一致。
02
恒河猴屏状体脑区与邻近脑区细胞类型的比较
为了比较 snRNA-seq 定义的屏状体细胞类型与岛叶、壳核和杏仁核中的细胞类型(图 2A),他们对恒河猴杏仁核(44967 个细胞)、岛叶(76527 个细胞)和壳核(39439 个细胞)的细胞进行了 UMAP 聚类,并使用已知标记对聚类进行注释。为了保持一致性,他们使用来自同两个恒河猴捐赠者的细胞,将每个区域下采样至约 15000 个细胞。对合并的细胞进行整合聚类分析显示,大多数聚类包含来自所有四个区域的细胞,尽管相对贡献不同。总体而言,屏状体聚类与岛叶聚类的相似性高于与壳核或杏仁核聚类的相似性(图 2B)。
通过对细胞类型重叠评分热图可视化,对屏状体与三个相邻脑区进行基于转录组的细胞类型共现分析(图2C),结果表明,屏状体中的谷氨酸能细胞类型与岛叶中的谷氨酸能细胞类型比与杏仁核中的谷氨酸能细胞类型更相似,而四个脑区的 GABA 能细胞和非神经元细胞均相似。平均重叠评分显示,屏状体与其他三个脑区之间的相似性因细胞亚类而异——所有岛叶亚类均相似,但只有部分杏仁核亚类与屏状体中的相似(图 2D)。进一步比较屏状体和岛叶之间的谷氨酸能细胞类型,方法是使用岛叶注释重新注释屏状体细胞(图 2E)。 GLUT/GNB4 亚类注释为 L5/6 端脑内 (IT) Car3 岛叶细胞,少数细胞映射到 L2/3 IT 细胞。近一半的 GLUT/RGS6 亚类与 L5 IT 和 L6 IT 岛叶细胞匹配,而几乎所有的 GLUT/ZFPM2 亚类都与 L6 皮质丘脑 (CT) 和 L6b 岛叶细胞匹配。有趣的是,绝大多数(86.4%)屏状体谷氨酸能细胞与深层(L5/6)岛叶细胞相似,这支持了屏状体和岛叶之间的发育关系。
他们进一步分析屏状体和 7 个皮质区域之间的重叠分数,结果表明,所有这些皮质区域中都存在屏状体谷氨酸能亚类。然而,屏状体的 GNB4 GLUT 亚类与岛叶的相似度高于与其他皮质区域的相似度。此外,谷氨酸能亚类和 GABA 能亚类在屏状体和岛叶之间的基因表达谱中表现出最高的相关性。有趣的是,表达神经肽 Y (NPY) 的 GABA/SST 细胞(称为长距离投射 GABA 能神经元)的百分比在屏状体中远高于所有皮质区域(图2F),这表明屏状体的抑制输出更显著。最后,他们表征了端脑不同脑区的神经元多样性,包括岛叶以外的6个皮质区域以及不同的端脑皮质下区域,包括屏状体、杏仁核、壳核、尾状核、苍白球外区(GPe)、苍白球内区(GPi)、伏隔核(NA)、无名质和迈纳特基底核(SI/NBM)以及海马。总体而言,屏状体的细胞特征更接近于皮层神经元,而非皮层下神经元(图2 G)。
对恒河猴、狨猴和小鼠屏状体分别进行 UMAP 聚类分析,结果显示恒河猴有 48 种细胞类型(图 S1 C),狨猴有 39 种细胞类型(109093 个细胞),小鼠有 60 种细胞类型(234986 个细胞)。使用恒河猴亚类注释对狨猴和小鼠细胞进行注释,进一步对这三个物种的混合细胞进行综合 UMAP 聚类。结果显示,三个物种之间各个亚类的相对丰度不同。对于谷氨酸能神经元,GNB4 亚类在恒河猴和狨猴中占主导地位,但在小鼠中仅占少数(14.7%)(图 2H),其中 ZFPM2 亚类更为丰富。对于 GABA 能亚类,LAMP5/LHX6 和 VIP 在恒河猴中表达最多,在狨猴中较少,在小鼠中最少(图 2 H)。跨物种比较所有16个屏状体亚类的标记基因,发现存在大量物种特异性标记基因——2551个基因为单一物种所独有,912个基因为两个物种共有,518个基因在三个物种中均有表达。这一发现与此前报道的各类皮层细胞基因表达的跨物种变异相一致。
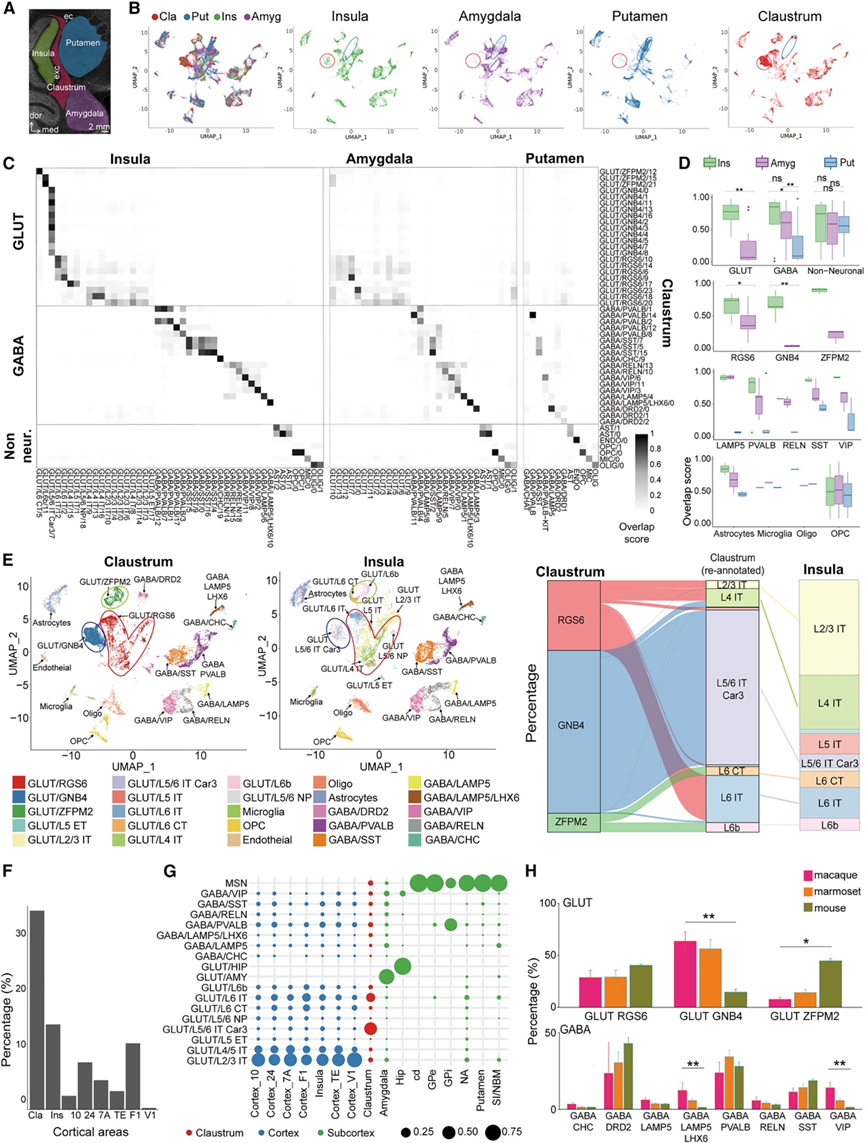
图2. 转录组定义的屏状体与邻近脑区的细胞类型以及细胞类型的跨物种比较。
(A) 冠状切面显示了屏状体和邻近脑区的相对位置。(B) 基于来自屏状体、岛叶、杏仁核和壳核的所有细胞的 snRNA-seq 数据对细胞聚类进行 UMAP 分析,以及从每个大脑区域提取的细胞图谱。(C) 屏状体与三个相邻脑区之间所有细胞类型的成对重叠得分。(D) 箱线图显示了 (C) 中的屏状体与其他三个大脑区域之间的重叠得分平均水平。(E) 恒河猴屏状体细胞(左)和岛叶细胞(中)谷氨酸能细胞亚类的对应关系(彩色圆圈标记)。桑基图显示了屏状体细胞和岛叶细胞(右)之间对应谷氨酸能细胞亚类的百分比。(F) 各皮质区域中表达NPY的生长抑素(SST)GABA神经元的百分比。(G) 来自不同大脑区域的 snRNA-seq 细胞的亚类分布。(H) 条形图显示恒河猴、狨猴和小鼠屏状体中各神经元亚类的比例。
03
恒河猴屏状突边界的划定
恒河猴的屏状体由 ec 和 exc 划分(图 2 A)。与以前的研究一致,他们发现了许多屏状体标记基因(如 SYNPR、NR4A2 和NTNG2)将屏状体与周围结构区分开来(图3 A)。此外,全基因组空间转录组图谱显示,存在一个明显的边界,该边界将屏状体本身与具有差异基因表达的区域分开,这里定义为“与腹内侧屏状体接壤的区域”(RBC)(图 3 B)。RBC 高表达CPLX3、CABP7和SULF1,但没有表达上述屏状体标记基因(图 3 A)。RBC区域在中部屏状体切面最为明显。在更靠近喙部的切面中,更扩张的RBC将屏状体与背侧内梨状核(DEn)分隔开来,DEn 也高表达常规屏状体标记基因SYNPY、NR4A2和NTNG2(图3A)。他们进一步确定了在屏状体、RBC 和 DEn 中高表达的基因,并将它们与岛叶、壳核、杏仁核和白质(“exc” 和“ec”)中的表达水平进行了比较(图 3 C)。RBC 的整体基因表达模式与屏状体有显著不同,而大多数在 DEn 中高表达的基因在屏状体中也高表达(图3C)。他们进一步确定了一组在屏状体中高表达但在 DEn 中不表达的基因,例LXN、SMYD1、GAL和TFAP2D。虽然 DEn 中TTN和SLC17A8的整体Z评分远高于屏状体,但进一步分析发现,这些基因在腹侧屏状体中具有相当的表达水平。值得注意的是,许多 RBC 富集基因,如CPLX3、CTGF、SULF1和NNAT,之前确定为小鼠屏状体皮质 L6b 或“壳”区域的标记基因。因此,他们认为 RBC 类似于小鼠的“屏状体壳”或“亚板”,但它不是恒河猴屏状体的组成部分。
沿背腹轴和内外轴定量了每个立体测序切片中各种细胞类型的分布(图 3D),将分布模式描述为均匀分布、内外偏好、背腹偏好或两者兼而有之。大多数谷氨酸能细胞类型分布不均匀,而几乎所有 (16/17) GABA 能细胞类型均均匀分布(图3E)。对于非神经元细胞类型,少突胶质细胞和星形胶质细胞(星形胶质细胞/1)显示优先分布,而 OPC、小胶质细胞和内皮细胞均均匀分布。四种谷氨酸能细胞类型示例说明了沿吻尾轴的切片内外偏好和背腹偏好的一致性(图 3F)。各种谷氨酸能细胞类型的空间组织在屏状体中高度结构化,暗示它们与不同脑区存在不同的输入和输出连接,而GABA能细胞类型的均匀分布则表明,神经元介导的局部回路在屏状体中相对均匀,观察到的少突胶质细胞的优先定位可能反映了整个屏状体中白质分布的异质性。
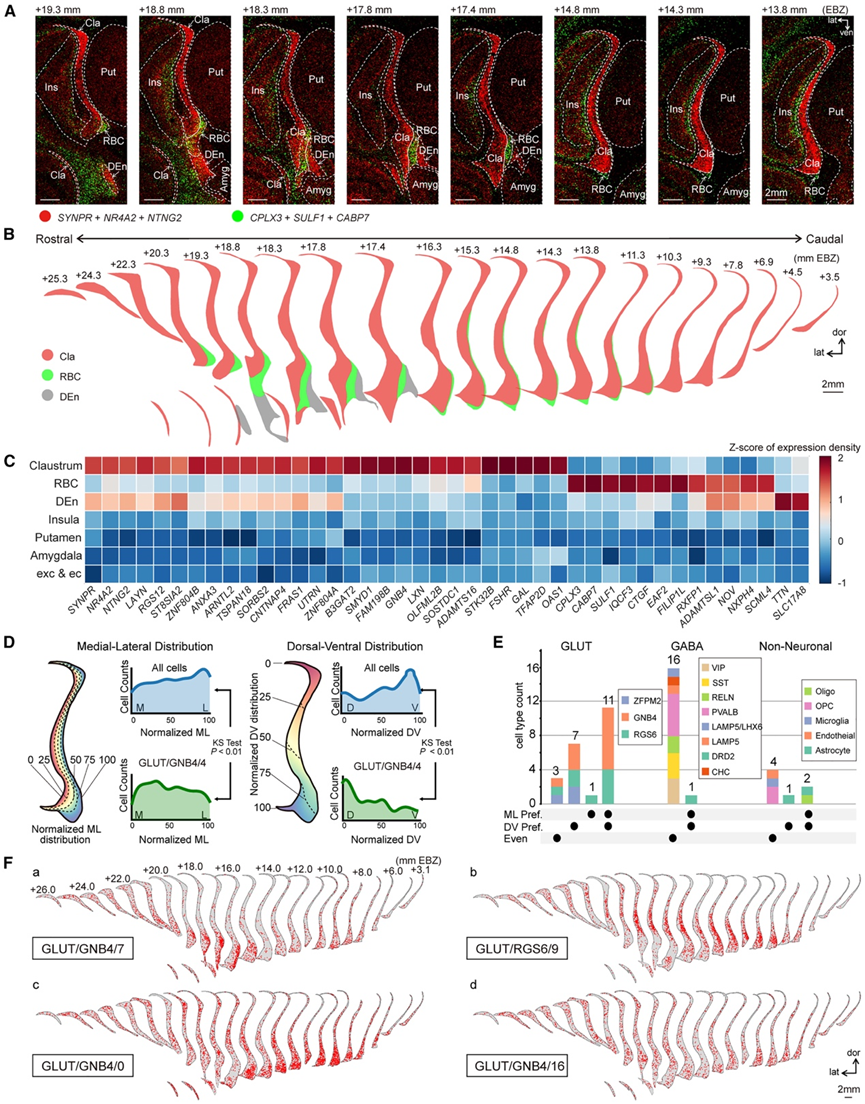
图3. 恒河猴屏状体的划分和细胞类型组织。
(A) 屏状体基因表达谱的空间模式,通过将屏状体8个冠状切面上6个代表性基因的表达水平相加而得出。(B) 基于转录组谱的三个独立区域的示意图。(C) (B)中三个区域和相邻大脑区域的标准化基因表达水平的热图。(D) 屏状体冠状切面标准化过程的示意图和细胞类型分布的统计分析。(E) 图表展示了细胞类型在内侧-外侧(ML)轴或背腹(DV)轴上的分布模式。(F) 空间图显示了屏状体中谷氨酸能细胞类型的四种典型分布模式。
04
屏状体投射神经元独特的目标依赖性分布
为了检查投射到不同皮质区域的屏状体细胞的空间组织,他们在 156 个间隔较大的位置注射逆行示踪剂(FastBlue 或 Diamedino Yellow,蓝色;霍乱毒素亚基 B [CTB] 与 Alexa 555 [CTB555] 结合,黄色;CTB488,绿色;CTB647,红色)后绘制了标记神经元的体细胞分布,覆盖 67 个皮质区域(图 4 A)。通过免疫染色 RBC 标志物晶体蛋白 mu (Crym)和 RNAscope 分析腹侧屏状体标志基因TTN和 RBC 标志基因CPLX3确定 RBC 和屏状体之间的边界。对 4 个皮质注射示例绘制了同侧屏状体中的标记神经元(图 4 B)。他们根据每次皮质注射的标记神经元的分布,通过核密度估计方法进一步定义了逆向标记的封闭体细胞“分布区”(DZ)。
他们对所有 67 个注射皮质区域的 DZ 进行了层次聚类,每个区域选择一种典型的注射。这揭示了 4 个 DZ聚类,反映了投射到四个不同皮质区域聚类的屏状体神经元的分布(图 4 C),标记神经元的四个示例分布与这四个聚类中的每一个相对应。对所有 156 个皮质注射标记的细胞的 DZ 进行更细粒度的聚类分析也发现了类似的四个聚类。然后,他们汇集了属于同一聚类的所有标记细胞,并定义了四个总体“投射选择区”(PSZ,1-4)。四个 PSZ 的合并图显示,这些 PSZ 在空间上是不同的,但 PSZ1 与其他三个 PSZ 部分重叠(图 4 E)。绘制了用四种不同颜色标记了各个 PSZ 中的闭壳神经元的注射部位(图 4A)表明 PSZ1 中的神经元主要投射到前额叶、联想叶和边缘叶皮质,而 PSZ2 神经元主要投射到早期视觉区(V1、V2 和 V4)。高度定位的 PSZ3 神经元投射到内嗅皮层(ENTO)、眶前等皮质区(OPRO)、颞极区(POLE)和颞上多感觉区(STPr)。PSZ4 神经元主要投射到额叶运动区和顶叶感觉区。值得注意的是,四个 PSZ 中的神经元投射到四个相对紧凑的皮质区域组,这些区域在等皮质平面图(图 4A)上大致隔离,并且大致对应于视觉系统中的不同层级。因此,PSZ3 和 PSZ2 屏状体神经元分别投射到高级和低级皮质区域(图4F)。
对63个皮层位点在对侧屏状体的标记神经元分布进行进一步绘图分析显示,虽然对侧屏状体神经元的投射强度(以标记神经元比例[FLN]衡量)普遍远低于同侧屏状体神经元,但大多数皮层区域(50/63)仍接收来自双侧屏状体的神经投射(图4G-H)。
他们在7个皮层下结构的15个位点注射了逆行示踪剂,发现丘脑、壳核、尾状核、海马体和杏仁核的注射位点均能在屏状体中标记出大量神经元,且这些神经元在屏状体内呈现注射位点特异性的分布模式(图4I)。进一步分析每个皮层下注射位点在四个PSZ分区中的标记细胞比例发现,皮层下投射神经元的分布与皮层投射神经元存在关联。例如,向壳核投射的屏状体神经元主要位于PSZ4区——该区同样包含主要投射至运动皮层区的神经元;而向海马投射的神经元则基本集中在PSZ3区——该区也是向ENTO皮层投射神经元的富集区(图4J)。这表明,每个PSZ分区包含的神经元会选择性投射至功能相关的皮层和皮层下结构,例如运动控制和记忆处理相关的脑区。
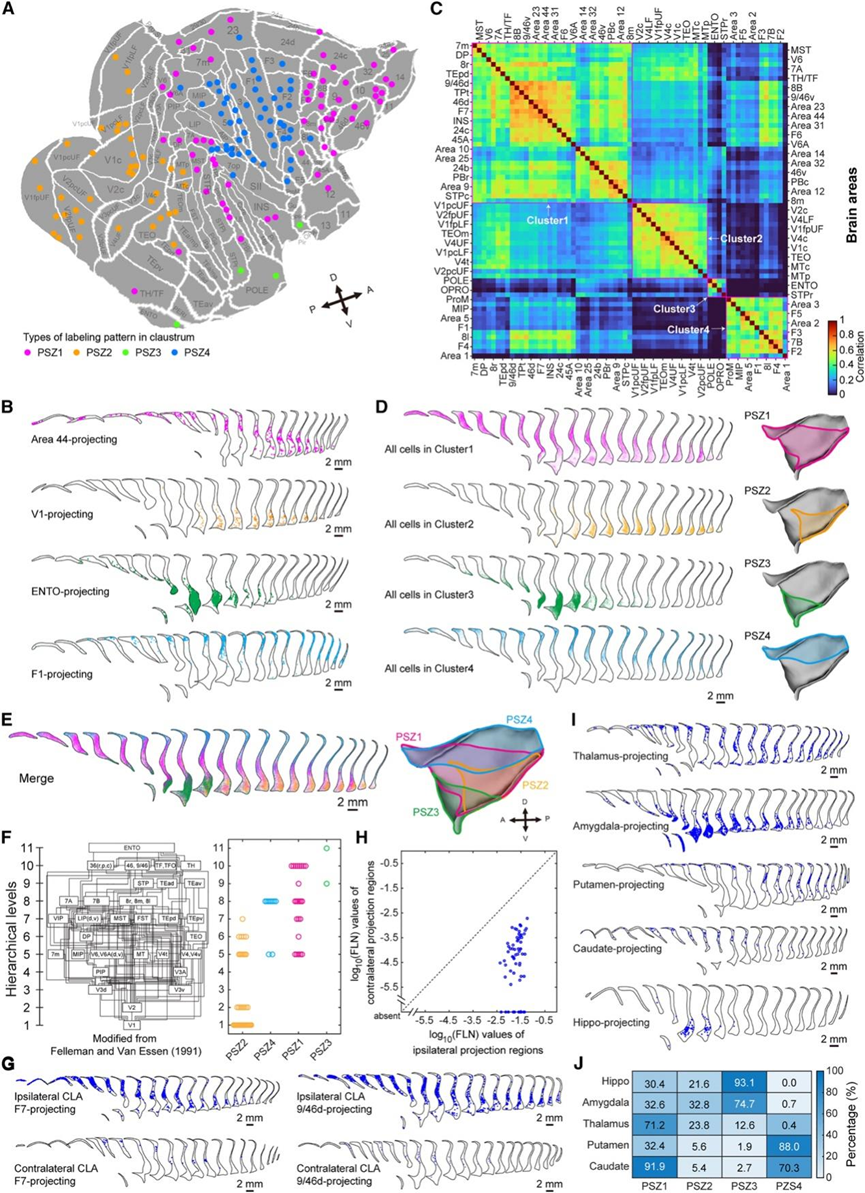
图4. 恒河猴屏状体向皮质和皮质下区域的投射。
(A) 示意图展示了平面恒河猴皮质图上的 156 个逆行示踪剂注射部位,每个部位均根据 (C) 中 DZ 的聚类分析以回顾性的方式进行颜色编码。(B) 通过在四个代表性皮质区域注射示踪剂标记屏状体内的体细胞分布投射神经元。 (C) 热图显示了67个皮质区域DZ成对相关性的层次聚类分析。(D) 由 (C) 图中四个神经元聚类定义的屏状体中的四个PSZ。(E) 四个 PSZ 的合并视图,每个 PSZ 中的标记神经元都用颜色编码。(F) 标记四个 PSZ 中的从句神经元的皮质注射部位(圆圈)根据其解剖层次进行分类。(G) F7(左)和 9/46d(右)中通过示踪剂注射标记的同侧(上)和对侧(下)屏状体中屏状体投射神经元的体细胞分布。(H) 同侧与对侧屏状体神经元向皮质注射部位(圆圈)的投射强度。(I) 通过注射标记的五个皮层下结构的屏状体投射神经元的分布。(J) 热图显示了(I)中五次皮层下注射后不同 PSZ 中标记神经元的百分比。
05
皮质和皮质下投射至恒河猴屏状体
为了将来自不同皮层和皮层下区域的输入映射到屏状体,他们在位于屏状体不同区域的五个位点(C1-C5)注射了逆向示踪剂(图5 A)。结果表明,C1、C2、C3 和 C5 注射的示踪剂摄取区严格局限于屏状体,而 C4 注射的示踪剂摄取区则包含一些局部白质。对逆向标记神经元进行全脑映射显示,五种屏状体注射导致皮层和皮层下区域标记神经元的特定模式。
在注射侧同侧皮层区域中,C1注射所标记的神经元主要分布在前额叶、额叶运动区、边缘系统和颞叶皮层(图5B-C)。C2注射标记的神经元皮层分布与C1相似,但在高级视觉区观察到更多标记细胞。与C1和C2相比,C3注射在高级视觉区产生的标记神经元密度显著更高,而在前额叶皮层则较少。C4注射标记的皮层神经元数量相对较少,且几乎全部集中在额叶运动区和顶叶感觉区(图5B-C)。值得注意的是,C4注射位点位于屏状体最背侧端——该区域特异性包含投射至运动区和体感皮层的神经元(图4A-D)。同样,位于腹侧中部的C5注射位点则包含投射至腹侧颞叶和前额叶皮层(包括ENTO和POLE区)的神经元(图4A-D)。因此,与近期小鼠研究结果不同,并非所有屏状体注射都会在同侧前额叶皮层产生密集标记,这表明屏状体不同功能域包含的神经元具有特定的同侧皮层输入-输出组合模式。
通过整合全部五次注射实验的标记神经元数据,他们发现屏状体接收来自同侧几乎所有皮层区域的强烈输入(初级视皮层V1和1区部分区域除外)(图5D),这一结果与既往研究一致。由于屏状体神经元对V1和1区存在显著投射,恒河猴屏状体与这两个皮层区域之间的连接主要表现为单向性,这一结果验证了屏状体对V1和1区具有自上而下调控作用的观点。对注射屏状体对侧皮质区域的标记神经元进行定位,结果显示标记细胞的密度总体低于同侧同域区域的密度(图5 E)。这些观察结果与啮齿动物的发现形成了鲜明对比。在啮齿动物中,对于一些皮质区域,屏状体的对侧输入可能强于同侧同域输入。因此,恒河猴屏状体的皮质输入存在明显的同侧偏向。
五次屏状体内注射导致 100 个同侧皮层下核标记,尤其是在杏仁核和丘脑中(图5 F)。投射到 C1、C2 和 C3 注射部位的同侧皮层下核的模式不同,这与它们的皮层连接有关。与 C1 和 C2 注射相比,C3 注射标记了同侧丘脑后核中的更多细胞(图 5 F),尤其是丘脑枕核(Puli、Pull 和 Pulm)、内侧膝状体核(MGmc 和 MGpc)和外侧膝状体核 (LGN),这些皮层下结构与视觉区域和联想顶叶皮层表现出广泛的连接,并且也强烈投射到 C3 部位。
这三个注射部位的对侧皮层下输入也表现出显著差异。C2 和 C3 注射部位的输入由许多对侧皮层下结构组成,包括杏仁核基底外侧核、下丘脑、丘脑和脑干,而只有对侧下丘脑向 C1 注射部位发送投射。有趣的是,C4 注射部位仅接收来自丘脑的投射,包括腹后外侧核 (VPLo, VPLc) 和腹后内侧核 (VPM)(图 5 F),这两个部位都已知与躯体感觉皮层相连,而躯体感觉皮层也向 C4 注射部位发送投射。C5注射标记了同侧多个皮层下核团中的细胞,包括嗅核和海马(图5 F)。与C2和C3注射类似,C5注射也标记了对侧杏仁核中的细胞。值得注意的是,如上所述,C5注射部位还接收了来自颞叶皮层(包括ENTO)的投射,这些投射参与了与海马和杏仁核相关的记忆功能。因此,各个隔间域接收来自特定皮层下结构的输入,这反过来又部分反映了它们与皮层的连接。
屏状体内的连接在信息处理中起着重要作用,但尚未在灵长类动物中得到探索。使用如上所述的屏状体内注射,他们绘制了逆向标记神经元在屏状体所有冠状切面上的分布情况(图5G)。C1、C2和C3注射标记的神经元在屏状体喙-尾轴上的分布模式相似,并逐渐向背腹方向移动(图5G)。C4和C5注射标记的神经元也表现出明显的沿喙-尾轴的优先分布。综上所述,这些数据表明屏状体内存在广泛的喙-尾连接,这与在大鼠中的发现一致。
有趣的是,他们发现C1、C2和C3注射标记的神经元很少分布在尾部屏状体的背侧和中部屏状体的腹侧,C4注射标记的神经元很少位于腹侧屏状体,而C5注射标记的神经元在背侧屏状体中缺失(图5 G)。这些空间分布模式表明屏状体内连接具有区域特异性。此外,通过确定每个注射部位位于不同皮质PSZ的标记神经元百分比,他们发现C1-C3注射标记的屏状体神经元主要(>80%)位于PSZ1,而C4注射标记的神经元主要(>99%)位于PSZ4(图5 H)。因此,屏状体内的连接模式在一定程度上反映了屏状体皮质PSZ的不同,这再次暗示了恒河猴屏状体内存在不同的PSZ。
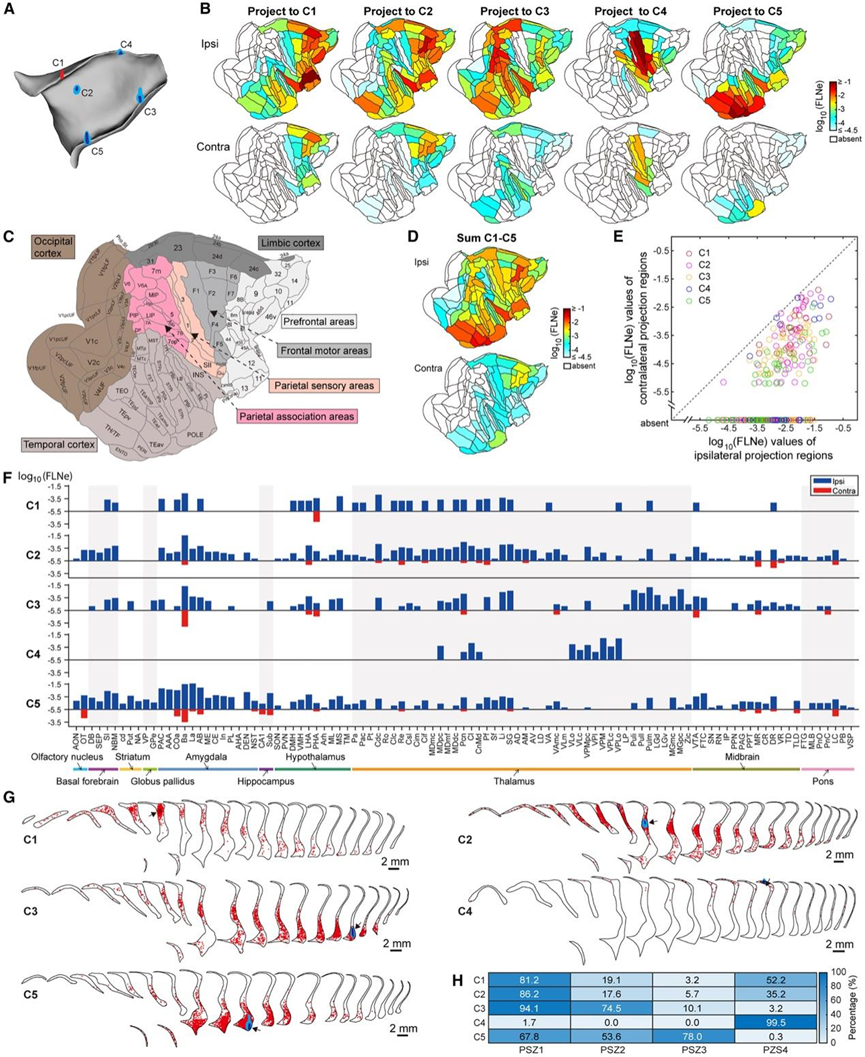
图5. 恒河猴屏状体的皮质和皮质下输入以及屏状体内的连接。
(A) 侧视图显示五个恒河猴屏状体注射位点(C1–C5)。(B) 平面图显示了五次屏状体内注射后同侧(顶部)和对侧(底部)皮质输入到屏状体的投射强度。(C) 平面图,描绘了(B)中广泛分类的皮质区域。(D) 平面图显示所有屏状体内注射的同侧(上)和对侧(下)皮质输入的总投射强度。(E) 五次屏状体内注射后同侧和对侧皮质区域的投射强度比较。(F) 条形图显示从不同皮层下区域到五个屏状体内注射点的投射强度。(G) 五次屏状体内注射标记的屏状体神经元的分布。(H) 热图显示了五次屏状体内注射后各个 PSZ 中标记神经元的百分比。
06
将转录组定义的细胞类型与投射靶向选择性神经元相匹配
他们进一步探讨了屏状体转录组定义的谷氨酸能细胞类型与其投射靶点之间的关系。首先在空间转录组图谱中确定了与屏状体投射神经元 DZ 相对应的区域(该 DZ 是通过在 156 个皮质(图 4 A)、9 个皮质下和 5 个屏状体内位点分别注射示踪剂来定义的)。分析了每个DZ 内各种屏状体谷氨酸能细胞类型的密度,然后确定了所有 DZ 中每种细胞类型的标准化密度。这样就可以比较 DZ 之间各种谷氨酸能细胞类型的密度差异(图 6 B)。各种细胞类型的标准化密度在属于四个聚类的 DZ 中显示出不同的模式(皮质区域列出的顺序与图 S4 I 相同)。例如,GLUT/RGS6/9 细胞类型在聚类1 的 DZ(包含主要投射到前额叶、联想和边缘区域的神经元)和聚类2 的 DZ(投射到视觉区域)中富集;GLUT/RGS6/14、GLUT/GNB4/7、GLUT/ZFPM2/15、GLUT/ZFPM2/21 和 GLUT/GNB4/2 细胞类型在聚类3 的 DZ(投射到 ENTO、OPRO、POLE 和 STPr)中富集;GLUT/GNB4/4 和 GLUT/GNB4/5 细胞类型在聚类4 的 DZ(投射到额叶运动区和顶叶感觉区)中富集。
此外,所有 4 个 PSZ 中谷氨酸能细胞类型的标准化密度(图 6 C)与聚类1-4 中这些细胞类型的平均密度非常相似(图 6 B)。这是预料之中的,因为不同 PSZ 的边界是由相应 DZ 聚类中合并的投射神经元的分布定义的。snRNA-seq 分析还验证了 PSZ1 至 PSZ4 之间的不同细胞组成。此外,即使对于在 PSZ 中均匀分布的细胞类型,也发现它们的基因表达模式不同。因此,由于谷氨酸能细胞类型的组成不同以及相同细胞类型的基因表达谱不同,不同的 PSZ 表现出不同的转录组谱。每个 PSZ 内不同类型的谷氨酸能投射神经元可能对其目标皮质区域进行不同的调节。
他们随后比较了皮层下投射的DZ和皮层投射的PSZ中的细胞类型组成。ENTO投射(PSZ3)和海马投射神经元,以及运动/躯体感觉皮层投射(PSZ4)和壳核投射神经元的各种神经元类型的标准化密度高度相似(图6C)。这表明重叠DZ中的同一组细胞类型负责靶向具有相关功能的大脑结构。
为了进一步研究特定DZ内转录组定义的谷氨酸能细胞类型是否确实优先投射到特定的皮质区域,他们将逆行示踪剂注射到ENTO皮质,并在注射染料12天后检测了屏状体切片,以识别由示踪剂逆行标记的空间转录组定义的细胞类型(图6D)。正如预期的那样,他们发现逆行染料标记的细胞基本上都位于腹侧屏状体的PSZ3内。Stereo-seq切片中所有染料标记的谷氨酸能神经元中各种谷氨酸能细胞类型的百分比(三个切片的平均值)与Stereo-seq切片中所有附近未标记的谷氨酸能神经元中各种谷氨酸能细胞类型的百分比非常匹配(图6E)。所有 PSZ3 细胞的细胞类型组成都能很好地代表逆向标记细胞的细胞类型组成,这一发现支持了以下观点:PSZ3 中几乎所有谷氨酸能细胞类型都是 ENTO 投射的。同样地,他们还将逆向示踪剂注射到初级运动皮层区域(图6F)、前额叶皮层和视觉区域,再次观察到立体测序切片中所有染料标记的谷氨酸能神经元中各种谷氨酸能细胞类型的百分比分布与附近未标记的谷氨酸能神经元的百分比分布相似(图 6G),尽管少数细胞类型(例如 GNB4/4)的百分比显示出相对较大的差异,表明在靶标方面存在细胞类型选择性。综合起来,这些结果表明,位于不同封闭区内的转录组定义的细胞类型的差异与皮层的不同目标选择性投射相关。
为了进一步研究参与屏状体内投射的谷氨酸能细胞类型,他们分析了五次屏状体内注射后DZ中谷氨酸能细胞类型的归一化密度。C1、C2和C3注射的谷氨酸能细胞类型分布相似,但C1-C3、C4和C5注射的谷氨酸能细胞类型分布差异很大(图6 B)。为了验证屏状体内注射特定DZ内计算出的转录组定义的谷氨酸能细胞类型是否确实优先投射到注射部位,他们将逆向示踪剂注射到腹侧屏状体,并鉴定了示踪剂逆向标记的空间转录组定义的细胞类型。在所有染料标记的谷氨酸能神经元中,各种谷氨酸能细胞类型的百分比与附近未标记的谷氨酸能神经元的百分比相似,这表明DZ内几乎所有谷氨酸能细胞类型都投射至注射部位。因此,转录组定义的不同细胞类型参与了不同的屏状体内连接。
他们对转录组定义的细胞类型进行的跨物种分析揭示了在恒河猴中富集的谷氨酸能神经元 GLUT/GNB4 亚类的存在。他们进一步检测了该亚类中的特定细胞类型是否表现出优先投射。首先绘制了恒河猴、狨猴和小鼠合并的 GLUT/GNB4 亚类细胞的 UMAP 聚类分布图(图 6 H)。然后,他们分析了恒河猴和小鼠 GNB4 细胞类型之间的重叠分数。最大重叠分数 <0.3 的细胞类型是“恒河猴特异性的”(图6I),而恒河猴和小鼠之间最大重叠分数 ≥0.3 的细胞类型是“恒河猴/小鼠保守的”。
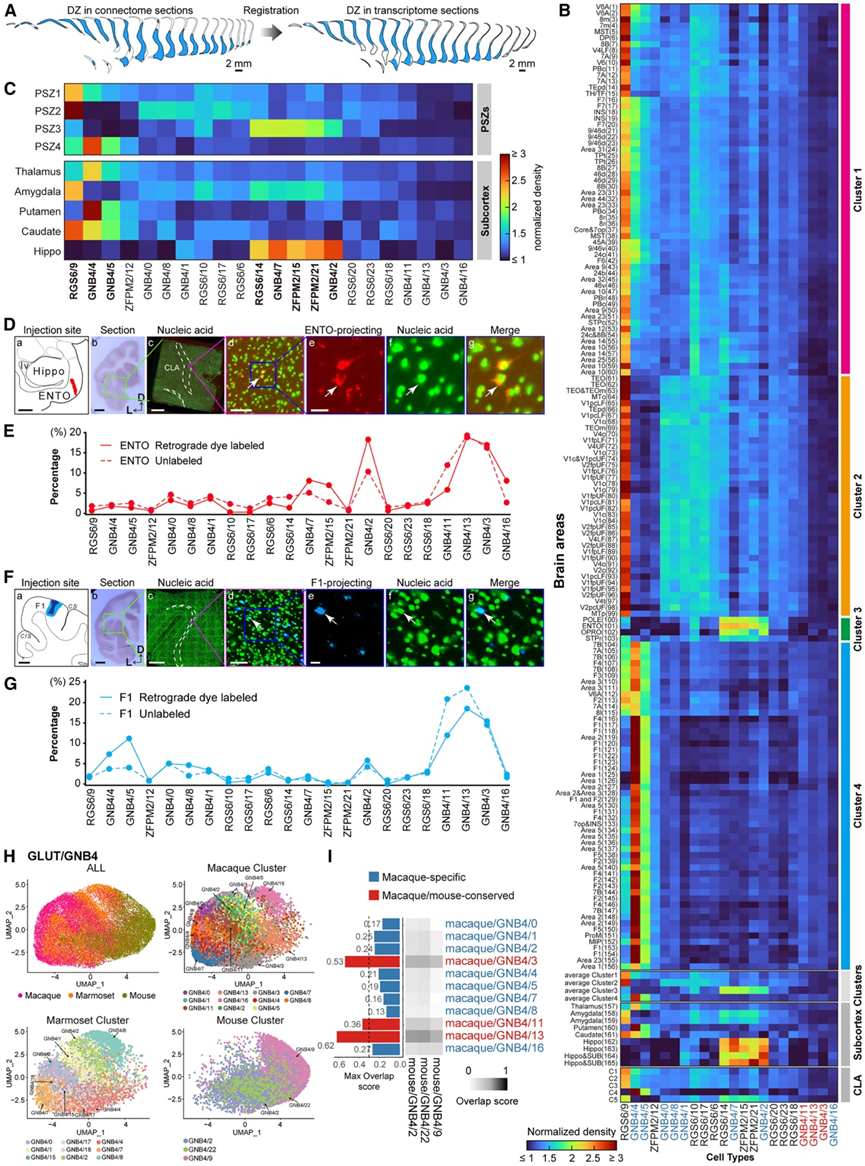
图6. 将转录组定义的细胞类型与投射靶点选择性神经元进行匹配。
(A) 将示例 DZ(左)注册到相应部分的 Stereo-seq 图上(右)。(B) 热图显示了 156 个皮质注射部位(按与图 S4 I相同的顺序排序并分为 1-4 聚类)中 DZ 内谷氨酸能细胞类型的标准化密度。(C) 热图汇总了4个PSZ(上)和5个皮层下结构DZ(下)中谷氨酸能细胞类型的平均归一化细胞密度。(D) 内嗅皮质(ENTO)注射逆行标记,结合Stereo-seq对封闭区细胞类型的映射。 (E) 内嗅皮质(ENTO)注射逆行标记,结合Stereo-seq对封闭区细胞类型的映射。(F) 初级运动皮层(F1)注射逆行标记,结合Stereo-seq技术对屏状体细胞类型进行定位。(G) 在 F1 中注射示踪剂后,逆向标记和未标记屏状体细胞的谷氨酸能细胞类型组成的标准化概况。(H) 从每个物种中提取的细胞 UMAP 图。(I) 右图:GLUT/GNB4 细胞类型的两两比较,显示恒河猴和小鼠之间对应的细胞类型。左图:直方图,显示恒河猴所有 GLUT/GNB4 细胞中 GLUT/GNB4 细胞类型的百分比。
+ + + + + + + + + + +
结 论
本研究对恒河猴屏状体细胞进行单细胞多组学分析,鉴定出48种转录组定义的细胞类型,其中大多数谷氨酸能神经元与深层岛叶神经元相似。通过比较恒河猴、狨猴和小鼠的转录组,揭示了恒河猴特异性的细胞类型。在67个皮质区和7个皮质下区进行逆向示踪剂注射,确定了四个不同的逆向标记屏状体神经元分布区。全脑连接和单细胞空间转录组的联合分析表明,这四个区域包含不同组成的谷氨酸能(而非GABA能)细胞类型,并优先连接到具有强烈同侧偏好的特定脑区。几种恒河猴特有的谷氨酸能细胞类型,分别位于腹侧和背侧的封闭区,选择性地共同投射到两个功能相关的区域——内嗅皮质和海马体,以及运动皮质和壳核,这些数据为阐明不同屏状体功能的神经元组织提供了理论基础。
+ + + + +



 English
English


