文献解读|Cancer Cell(44.5):基于蛋白质的分类揭示了IDH突变型星形细胞瘤的免疫热亚型,其预后较差
✦ +
+
论文ID
原名:Protein-based classification reveals an immune-hot subtype in IDH mutant astrocytoma with worse prognosis
译名:基于蛋白质的分类揭示了IDH突变型星形细胞瘤的免疫热亚型,其预后较差
期刊:Cancer Cell
影响因子:44.5
发表时间:2025.09.11
DOI号:10.1016/j.ccell.2025.08.006
背 景
异柠檬酸脱氢酶 (IDH) 突变型星形细胞瘤是一种侵袭性强、可塑性高的脑肿瘤,患者在接受标准治疗后几乎不可避免地会复发。自 2021 年世界卫生组织 (WHO) CNS5 分类以来,它已确认为成人弥漫性胶质瘤的三种分子亚型之一。虽然分子诊断改善了患者的治疗管理,但 IDH 突变型星形细胞瘤仍然是一种致命性疾病,其治疗结果差异很大,这主要归因于肿瘤的异质性和复杂的潜在分子机制。为了阐明胶质瘤的异质性,大量资源已被投入到癌症基因组和转录组的测序中。cIMPACT-NOW联盟总结了多项研究,推荐CDKN2A /B纯合缺失作为IDH突变型星形细胞瘤的WHO 4级标准。最近的纵向测序分析进一步表明,MYC扩增(例如CDKN2A/B纯合缺失)可预测IDH突变型星形细胞瘤的侵袭性进展。然而,对于缺乏这些改变的患者,其疾病进展和耐药机制仍知之甚少。
实验设计
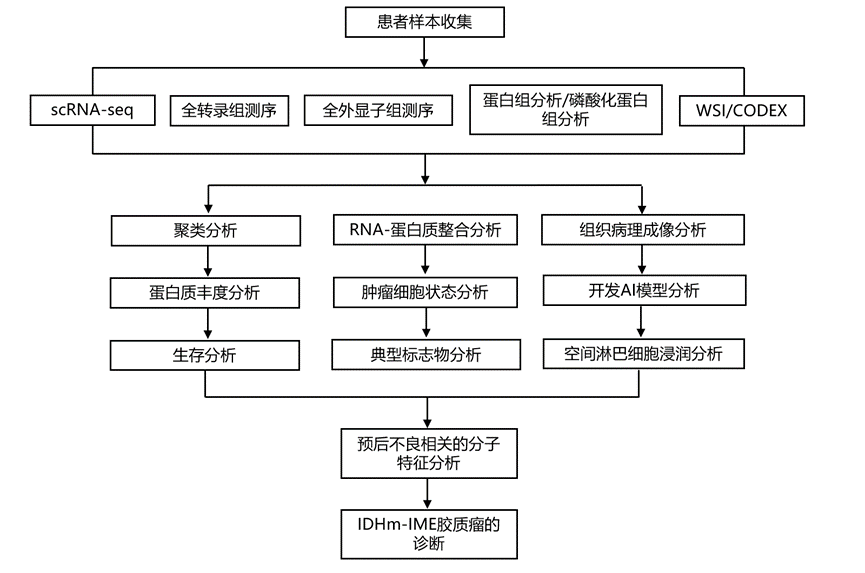
结 果
01
IDH突变型星形细胞瘤的蛋白质簇与不同的生存结果相关
研究团队收集了来自 51 例成人弥漫性 IDH 突变型星形细胞瘤患者的多组学数据:51 例进行了蛋白质组学分析,40 例进行了全转录组测序 (WTS),41 例进行了磷酸化蛋白质组学分析,39 例进行了全外显子组测序 (WES),39 例进行了 DNA 甲基化微阵列分析,31 例进行了病理全切片成像 (WSI),21 例进行了单细胞转录组分析(scRNA-seq)。此外,他们还纳入了两个纵向队列,共包含 189 对肿瘤样本,用于研究其进化动态,其中 60 对样本进行了WTS分析,129 对样本进行了 WSI 分析。利用 10× Visium HD 技术,生成了 214403 个细胞中 18805 个基因的空间分辨表达谱。为了验证结果,他们构建了两个独立的临床队列,共包含 507 例 IDH 突变型星形细胞瘤及其转录组谱,并生成了基于索引的共检测(CODEX)数据,该数据捕获了3283124个细胞的单细胞空间蛋白表达模式(图 1A)。这一全面的数据集能够识别和表征具有临床意义的 IDH 突变型星形细胞瘤亚群。
他们对蛋白质组学数据进行了无监督聚类,并鉴定出四个聚类:IDH突变型脂肪生成/脂肪酸代谢聚类(IDHm-AFM,绿色)、IDH突变型增殖/祖细胞聚类(IDHm-PPR,红色)、IDH突变型免疫/间质富集聚类(IDHm-IME,橙色)和IDH突变型神经元聚类(IDHm-NEU,蓝色)(图1 B)。AFM聚类显示出广泛的代谢程序(脂质、羧酸和硫代谢),其中脂肪生成和脂肪酸代谢是其标志。PPR聚类富集细胞周期、DNA复制和增殖。IME聚类的特征是干扰素-γ反应和上皮-间质转化(EMT)。NEU 富含神经元功能,包括神经元投射发育和突触传递。
整合匹配的临床数据、基因组突变和拷贝数变异(CNV)后,PPR 显示出CDKN2A/B缺失的高发率,并且富集 4 级和 IDH A 类甲基化、高级别胶质瘤(图 1B)。各组之间的总生存期(OS)和无进展生存期(PFS)存在显著差异(图 1C)。PPR的预后较差,这与其CDKN2A/B缺失的高发率和 4 级肿瘤富集相一致。值得注意的是,IME缺乏上述模式中的已知标志物,但其预后同样较差,这凸显了蛋白质组学在定义 IDH 突变型星形细胞瘤中具有临床意义的亚聚类方面的实用性。
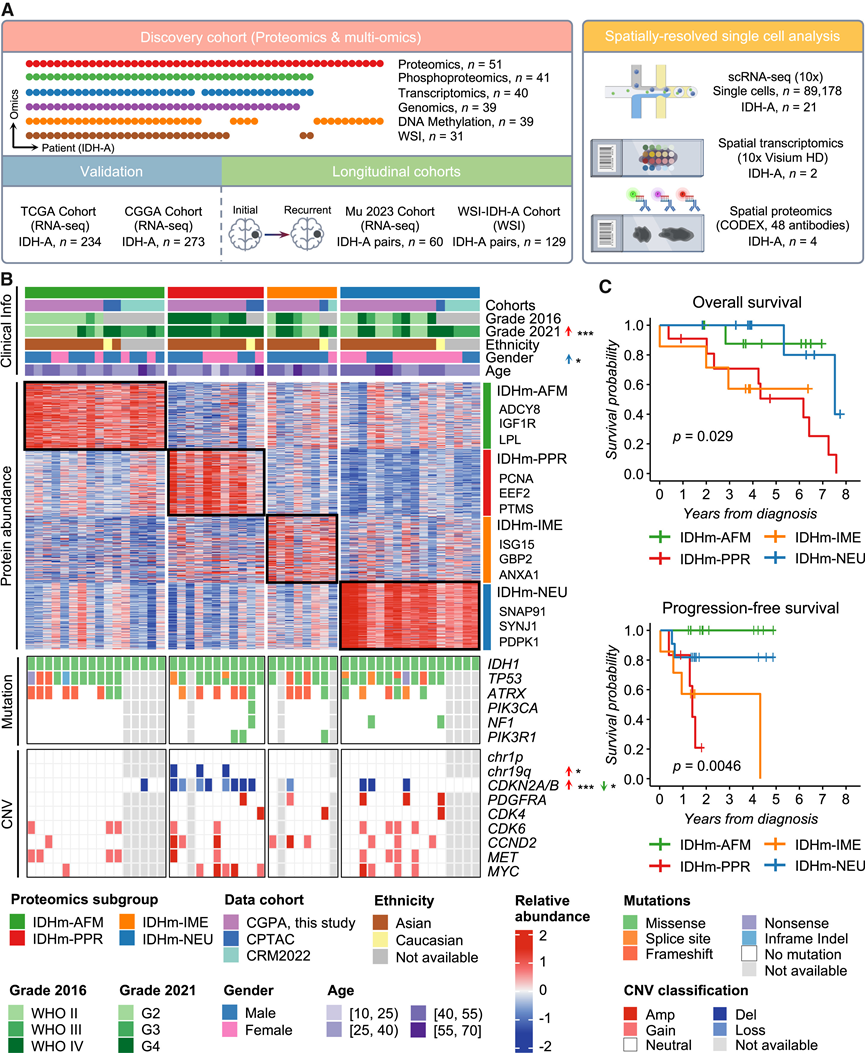
图1. IDH 突变型星形细胞瘤的蛋白质聚类与不同的生存结果。
(A) IDH 突变型星形细胞瘤的蛋白质聚类与不同的生存结果。(B) 使用非负矩阵分解 (NMF) 对 51 名 IDH 突变型星形细胞瘤患者进行蛋白质丰度无监督聚类。(C) 使用NMF对 51 名 IDH 突变型星形细胞瘤患者进行蛋白质丰度无监督聚类。
02
综合分析验证了蛋白质聚类在不同队列中的预后价值
对 mRNA 数据进行主成分分析 (PCA) 表明,基于转录组学的无监督方法无法区分蛋白质聚类。差异蛋白质组分析定义了亚型特异性蛋白质特征。不出所料,这些特征的 mRNA 表达在区分这些蛋白质聚类方面的能力有所降低。例如,富含半衰期较短的细胞外蛋白的 IME 聚类的蛋白质特征在 mRNA 水平上的倍数变化显著降低。为了对仅包含转录组学数据的队列进行分类,他们开发了一种基于转录组学的分类器,用于区分AFM、PPR、IME和NEU。具体而言,他们利用队列中匹配的蛋白质组学-转录组学数据,定义了每个蛋白质聚类的RNA特征,并进行了Mann-Whitney-Wilcoxon基因集检验以对样本进行分类。该分类器通过留一交叉验证获得了较高的平衡准确率(图2A)。值得一提的是,尽管存在差异,IME的RNA特征与蛋白质特征在统计学上相关,尤其是在免疫和间充质通路中(图2B)。
在癌症基因组图谱(TCGA)IDH突变型星形细胞瘤中,4个IME组的OS与PPR组相似,但劣于AFM/NEU组(p = 0.029)。在校正肿瘤分级、年龄和性别的多变量Cox模型中,IME组仍然是预后不良的独立预测因子,而PPR组则失去了显著性,这与其在4级肿瘤中的富集相一致。在中国胶质瘤基因组图谱(CGGA)研究中,经过长达 20 年的随访,IME 的 OS 再次表现不佳,与 PPR 相当,且显著差于 AFM/NEU(图 2C-D)。多变量模型证实 IME和 PPR是独立的生存预测因子(图 2E)。此外,各队列中蛋白质聚类的比例一致,IME 约占 12%–14%(图 2C)。
为了研究蛋白质定义聚类的演化动态,他们将分类器应用于60对初次发作-复发性IDH突变型星形细胞瘤。有趣的是,AFM分类器评分在复发时下降,而PPR、IME或NEU则无显著变化(图2F)。值得注意的是,匹配的初次发作和复发肿瘤的亚型转变显示,复发时AFM降低,而PPR和IME升高(图2G)。
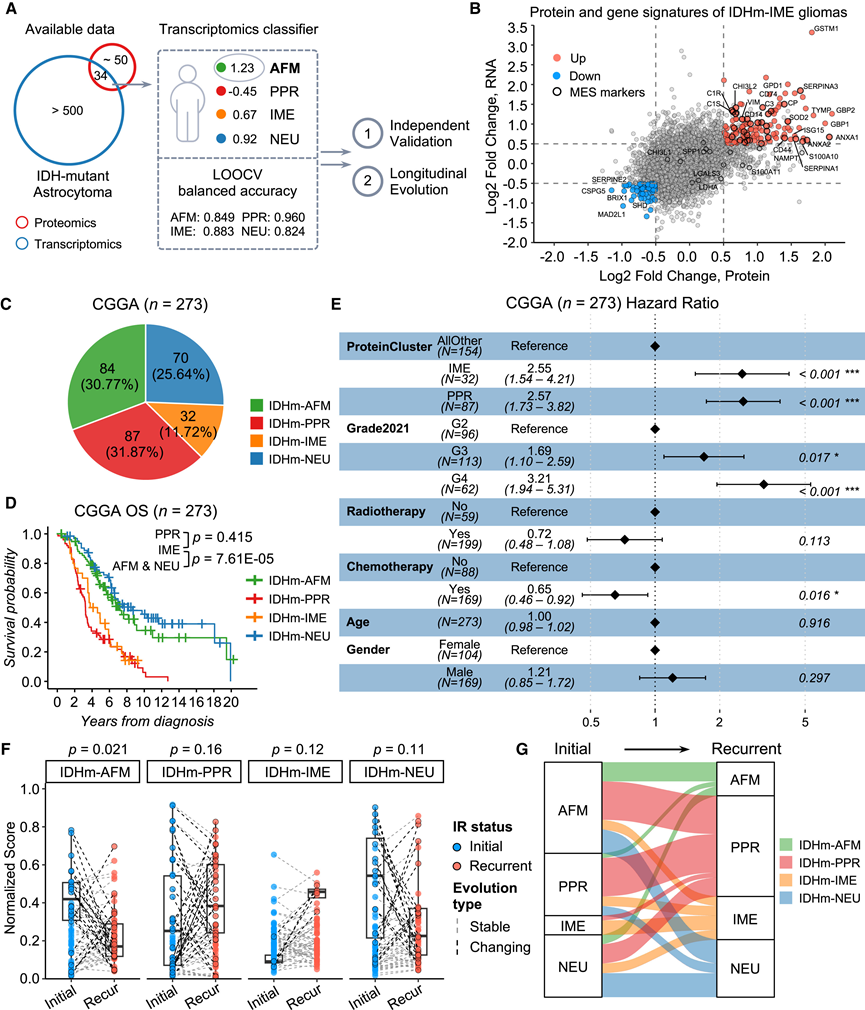
图2. RNA 和蛋白质的整合分析验证了多个队列中蛋白质聚集的预后价值。
(A) 实验流程。(B) 散点图显示了 IDHm-IME 亚组与所有其他 IDH 突变型星形细胞瘤之间转录组和蛋白质组改变的相关性。(C) 饼图显示使用转录组学分类器在独立 CGGA 队列中分类的蛋白质簇的百分比。(D) Kaplan-Meier 曲线显示 CGGA 中 IDH 突变型星形细胞瘤患者的总生存率。(E) 基于多变量Cox比例风险模型,森林图显示CGGA中IDH突变型星形细胞瘤患者的总生存期风险比(HR)。(F) 基于多变量Cox比例风险模型,森林图显示CGGA中IDH突变型星形细胞瘤患者的HR。(G) 基于多变量Cox比例风险模型,森林图显示CGGA中IDH突变型星形细胞瘤患者的HR。
03
单细胞分析揭示了IDHm-IME胶质瘤中明显的淋巴细胞浸润和增强的免疫活性
为了区分肿瘤内在信号和微环境信号,他们对来自18例患者的21个IDH突变型星形细胞瘤标本进行了scRNA-seq,这些标本均具有匹配的蛋白质组学数据(3例IME,5例AFM,3例PPR和7例NEU)。他们根据标记基因将总共89242个高质量细胞分为肿瘤细胞、髓系细胞、淋巴细胞和少突胶质细胞群(图3A),并通过检测拷贝数变异确认了肿瘤细胞。比较不同蛋白质聚类中的非恶性细胞,他们观察到IME中淋巴细胞的富集程度显著高于其他组(图3B-C)。
基于先前对IDH突变型星形细胞瘤转录状态的研究,他们重新分析了恶性细胞,并通过无监督聚类鉴定了六种肿瘤细胞状态:神经祖细胞样(NPC样)、MES样、AC样、OC样、G1/S期和G2/M期,这些状态由经典标记物进行注释(图3D)。大多数状态与已发表的癌细胞状态一致。在IDH突变型星形细胞瘤中新定义的MES样状态富集于免疫应答通路。值得注意的是,MES样和AC样状态在IME蛋白聚类中显著增加,而G1/S期和G2/M期状态则减少(图3E)。免疫细胞聚类分析鉴定出多种髓系细胞(中性粒细胞、单核细胞、巨噬细胞、小胶质细胞、树突状细胞)和淋巴系细胞(B细胞、浆细胞、CD4+T细胞、调节性T细胞(Treg)、CD8+ T细胞、自然杀伤T(NKT)细胞、CD56dim NK细胞和CD56 brigh NK细胞)。样本水平比例相关性分析显示,在IDH突变型星形细胞瘤中,MES样肿瘤细胞与巨噬细胞浸润相关。
接下来,他们比较了不同蛋白聚类的单细胞转录组数据,鉴定出肿瘤细胞和非肿瘤细胞群的典型标志物(图3F)。值得注意的是,IME肿瘤微环境(TME)中的淋巴细胞IGKC表达显著升高,表明浆细胞富集。对IME细胞群来源的特征基因进行可视化分析显示(图2B),干扰素刺激基因和CD74表达上调,其中GBP1和GBP2在MES样IME胶质瘤细胞中特异性升高(图3F,中)。免疫相关基因在髓系和 MES 样肿瘤细胞中表现出主要组织相容性复合体表达升高,并且在 IME 相关免疫细胞中免疫抑制介质(CD163和 TGFBI)、淋巴细胞效应因子(GZMK)和免疫球蛋白基因(IGHG1)上调(图 3 F,右)。
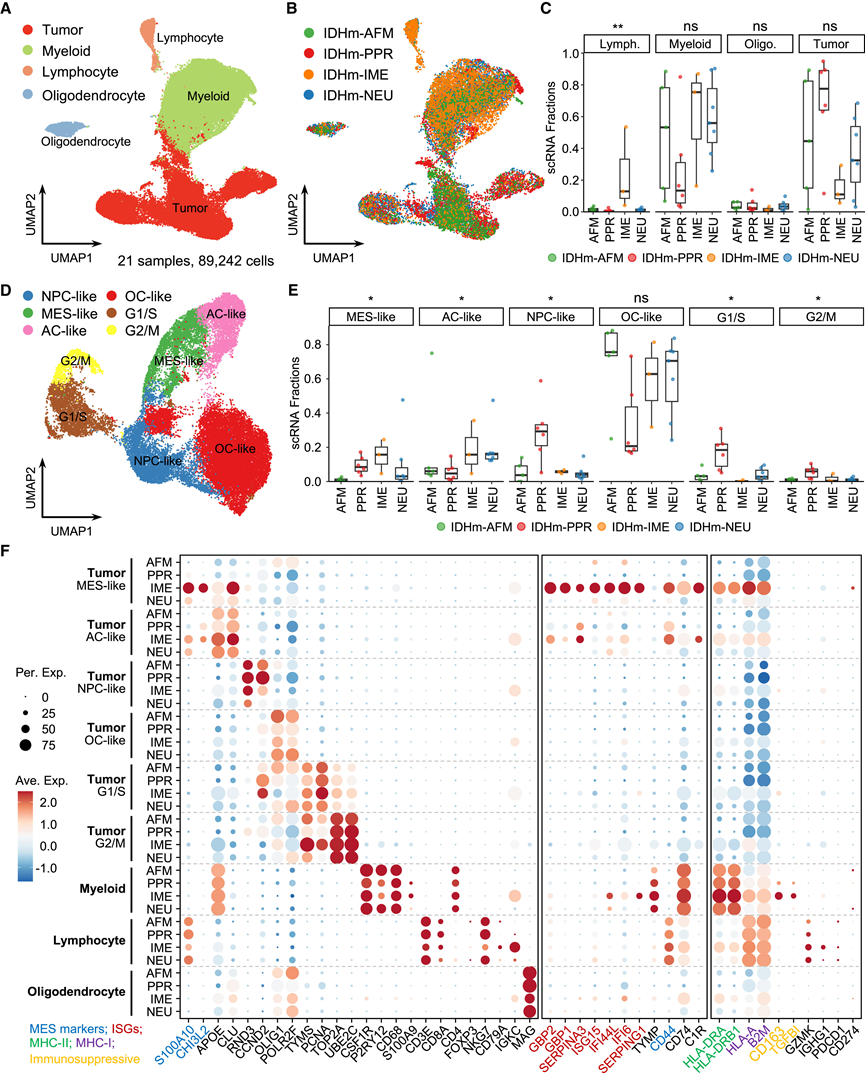
图3. 单细胞分析显示IDHm-IME胶质瘤中存在明显的淋巴细胞浸润和增强的免疫活性。
(A) 21 个 IDH 突变型星形细胞瘤的单个细胞的均匀流形近似和投影 (UMAP) 图。(B) UMAP 图显示了单个细胞在四个蛋白质组学亚组中的分布。(C) 四个蛋白质聚类中不同主要细胞类型的比例。(D) 21例IDH突变型星形细胞瘤肿瘤细胞的UMAP图。(E) 四种蛋白质聚类中不同肿瘤细胞状态的比较。(F) 不同主要细胞类型和肿瘤状态下选定基因的点图。
04
组织病理成像显示IDHm-IME胶质瘤中富含肥胖细胞分化
接下来,他们评估了四个蛋白簇的组织病理学特征。在IME中观察到了胶质细胞分化(GD),其特征是肿瘤细胞胞质增大、嗜酸性,且细胞核偏位(图4A)。在本研究的发现队列中,6/6例IME病例和3/29例非IME病例中均存在GD(图4B)。为了验证这一发现,他们开发了一个基于大型语言模型(LLM)的工作流程,用于从描述性文本中提取诊断细节和组织病理学相关特征。将该工作流程应用于TCGA IDH突变型星形细胞瘤病例的所有可获取的病理报告,证实了GD在IME中的富集(图4B)。同样的LLM辅助分析显示,PPR中存在频繁的坏死和高有丝分裂,与4级肿瘤富集相符。这些结果突显了IME中GD的独特富集,并证实坏死和有丝分裂是PPR的关键特征。
为了能够从常规病理图像中快速识别IME,他们开发了一种人工智能(AI)模型,利用WSI将患者分类为IDHm-IME(图4C),该模型与病理学家对肥胖细胞的定量分析结果高度相关(图4D),并且能够准确分类IME(图4E)。
为了研究胶质瘤演变过程中GD形态是否发生变化,他们构建了一个包含129对匹配的初发/复发IDH突变型星形细胞瘤的纵向WSI队列。两位病理学家手动确认了GD形态的进化保守性(图4F)。为了定量研究GD的演变,他们将AI模型应用于所有WSI配对样本,并计算了每个样本中GD斑块的百分比。有趣的是,虽然复发肿瘤表现出越来越多的IME表型,但GD的检出率在更高的胶质细胞阈值下反而下降(图4G)。这一看似矛盾的现象促使他们对配对的初发GD+/复发GD-样本进行了详细的组织病理学复查。有趣的是,他们发现复发时出现了肿瘤流(排列的梭形细胞),这在初发肿瘤中很少见(图4H),这解释了AI分类器对GD检出率降低的原因,并提示形态学进展而非胶质细胞丢失。
为了进一步研究这一现象,他们重新分析了60例匹配的初始/复发病例的RNA-seq数据。功能富集分析显示,复发性IDHm-IME胶质瘤中上调的通路富集于与胶原代谢和细胞外基质组织相关的过程(图4I)。此外,反卷积分析揭示了复发性IDHm-IME胶质瘤中成纤维细胞丰度显著增加(图4J),提示成纤维细胞可能是肿瘤演化的潜在驱动因素。与此一致的是,对组织病理学图像的人工复核证实,与其它病例相比,复发性IDHm-IME胶质瘤中纤维增生显著增加(图4K)。
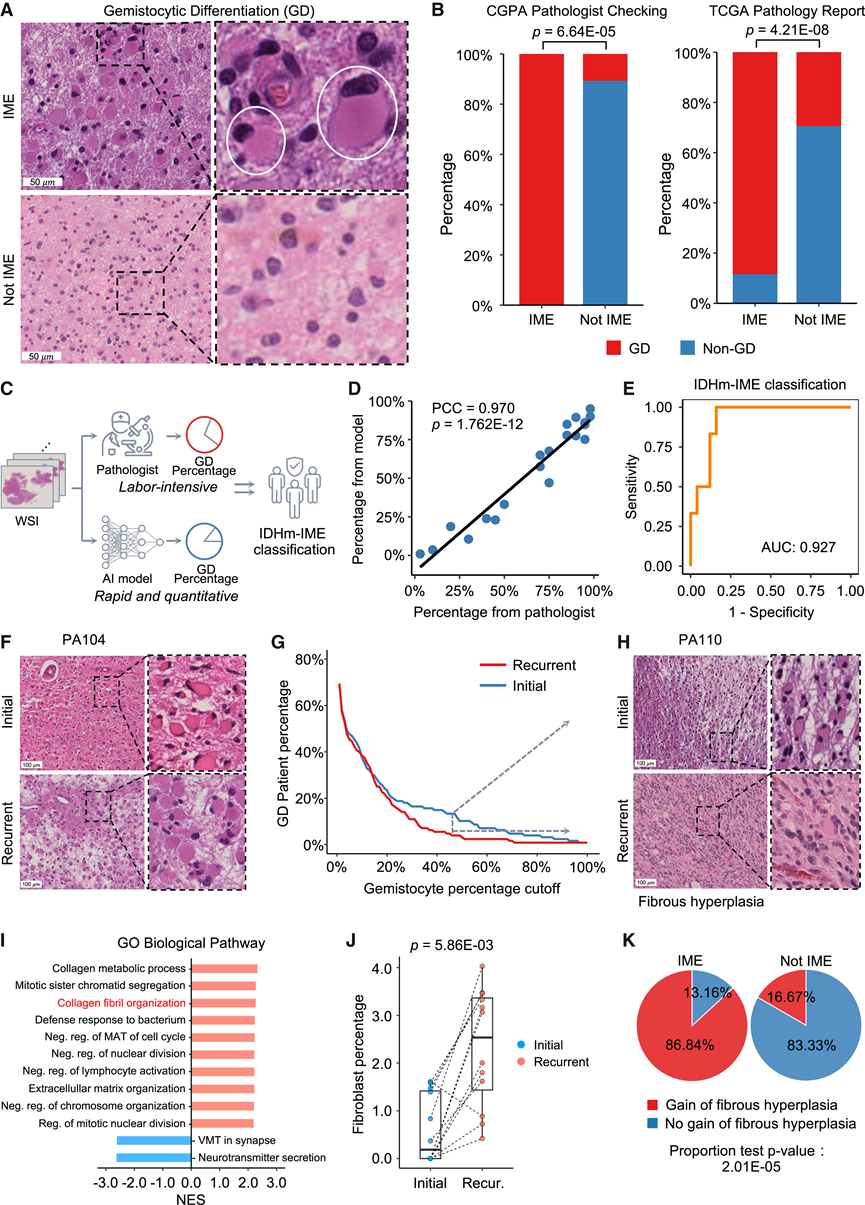
图4. 组织病理学成像分析显示 IDHm-IME 胶质瘤中存在丰富的生殖细胞分化。
(A) 代表性组织病理学图像显示IDHm-IME胶质瘤中存在生殖细胞分化。(B) 左图为病理学家手动检查的 CGPA 队列中 IME 亚组与其他 IDH 突变型星形细胞瘤患者的 GD 患者比例,右图为基于现有病理报告的 TCGA 队列中 IME 亚组与其他 IDH 突变型星形细胞瘤患者的 GD 患者比例。条形图显示各组中 GD 患者的百分比。p值通过单样本比例检验计算。(C) 通过快速定量估计WSI上GD肿瘤细胞百分比,开发AI辅助IDHm-IME分类工具的流程示意图。(D) 散点图显示了病理学家注释的 20 个训练 WSI 与 AI 模型估计的 GD 百分比之间的相关性。(E) 散点图显示了病理学家注释的 20 个训练 WSI 与 AI 模型估计的 GD 百分比之间的相关性。(F) 散点图显示了病理学家注释的 20 个训练 WSI 与 AI 模型估计的 GD 百分比之间的相关性。(G) 散点图显示了病理学家注释的 20 个训练 WSI 与 AI 模型估计的 GD 百分比之间的相关性。(H) 匹配的初始和复发性IDHm-IME肿瘤的代表性H&E染色组织病理学图。(I) GO 生物通路富集分析。(J) 匹配的初始和复发性IDHm-IME胶质瘤的反卷积成纤维细胞百分比比较。(K) 饼图比较了匹配的初始肿瘤和复发肿瘤中纤维增生增加的复发肿瘤样本比例。
05
IDHm-IME胶质瘤中肿瘤细胞状态和淋巴细胞浸润的空间动态
为了将GD形态与单细胞表达谱联系起来,他们利用10× Visium HD和CODEX对一对匹配的初发-复发IDHm-IME胶质瘤样本进行了空间分析。Visium HD能够实现单细胞尺度的空间转录组分析,且组织覆盖无间隙;而CODEX则提供了真正的单细胞蛋白水平空间分析。他们采用相邻切片法,为每个样本制备了三个相邻切片:中间切片用于苏木精-伊红(H&E)染色和Visium HD分析(图5A),其余两个切片用于CODEX分析(包含48个标记物的尾部标记物)和H&E染色,以全面分析肿瘤细胞状态和免疫微环境。
他们将 GD AI 分类器应用于 H&E 图像,以绘制高 GD 区域图,观察到初始样本几乎所有区域以及复发样本特定区域中均存在 GD 形态。根据这些图谱,他们进行了选择。6。5米米×6。5米米在两个样本中,Visium HD 均捕获了包含 GD 和非 GD 模式的区域。对 Visium HD 数据进行无偏空间聚类发现,初始样本中存在六个空间域 (SD),复发样本中存在七个空间域,形成层状结构(图 5 B),类似于 IDH 野生型 GBM 中报道的多层结构。对相邻 CODEX 切片的蛋白质谱分析显示,CD74 在 SD2-AC/MES 区域特异性富集(图 5 B,左侧和右侧),而 GD 细胞也聚集于此,这与单细胞分析中 CD74 作为主要 IME 标志物的结果一致(图 3 F)。
然后,他们使用人工智能驱动的工作流程从Visium HD区域提取单核表达谱,在初始样本中识别出53305个细胞,在复发样本中识别出160098个细胞。在先前10倍单细胞分析的指导下,他们注释了五种主要细胞类型(恶性细胞、髓系细胞、淋巴细胞、少突胶质细胞和血管细胞)和六种肿瘤细胞状态(AC样、MES样、OC样、NPC样、G1/S期和G2/M期)。为了探索这些细胞类型的空间组织,他们进行了细胞邻域分析,并确定了 10 个反复出现的细胞微环境:4 个恶性细胞占主导地位的微环境(微环境 4、5、6 和 7),2 个非恶性细胞占主导地位的微环境(微环境 9 和 10),以及 4 个混合的肿瘤-正常细胞微环境(微环境 1、2、3 和 8)(图 5 C)。
为了将GD形态与细胞状态相匹配,他们将AI分类器得到的GD评分与每个Visium HD图像块的无偏细胞状态注释进行关联。GD形态与MES样肿瘤密度显著相关(图5D),并且与3号微环境的MES样/淋巴细胞富集特征一致(图5C),GD区域也显示出淋巴细胞增多(图5E)。CODEX蛋白数据通过比较高GD评分区域和低GD评分区域验证了这些模式(图5F)。
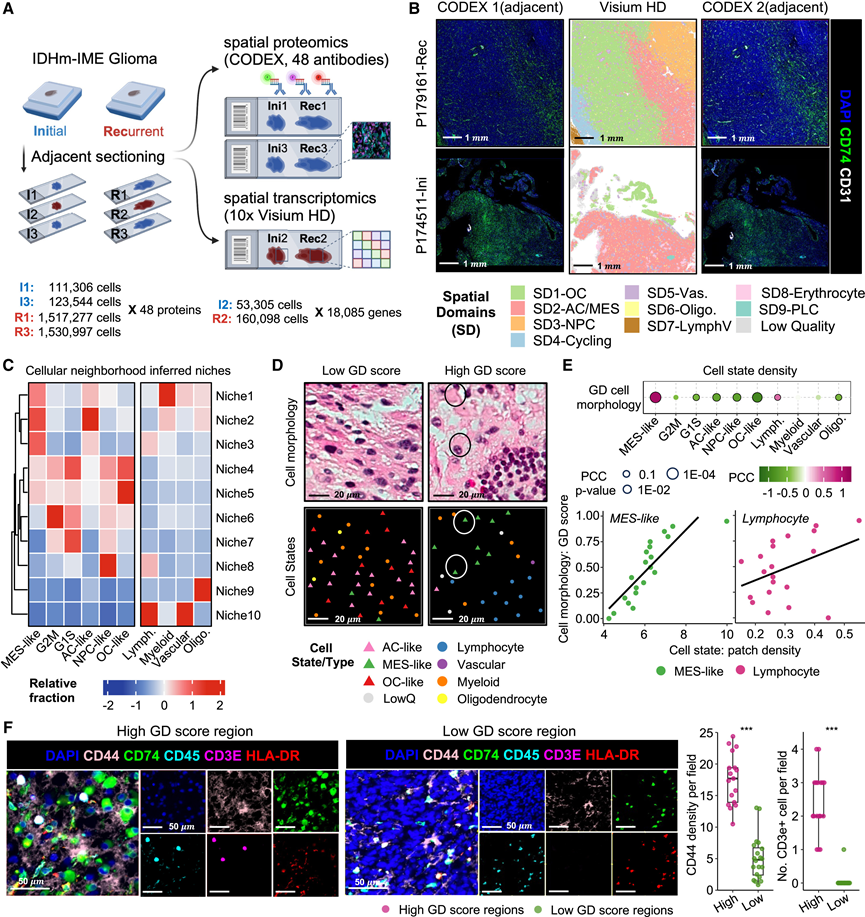
图5. IDHm-IME胶质瘤中肿瘤细胞状态和淋巴细胞浸润的空间动态。
(A) 空间多组学实验设计和样本信息。(B) Visium HD 捕获区域内 CODEX 1、Visium HD 和 CODEX 2 数据的空间匹配。(C) 热图显示了根据细胞邻域分析推断出的10种细胞类型/状态在10个细胞微环境内的共现情况。(D) 代表性图像显示两个示例斑块。(E) GD形态与肿瘤细胞状态和TME细胞类型的相关性。(F) IDH 突变型星形细胞瘤中高 GD 评分区域与低 GD 评分区域的代表性 CODEX 图像。
06
免疫热点IDHm-IME胶质瘤中的空间淋巴细胞浸润
为了探索调控IDH突变型IME胶质瘤复杂微环境的治疗靶点,他们重新审视了来自整体和空间单细胞多组学的关键发现。鉴于IME的免疫热点特征,他们利用空间单细胞蛋白质组学(CODEX)对免疫细胞进行了分析。先前一项研究报道了肥胖细胞和血管周围淋巴细胞套袖(PLC)的共存,他们也在发现队列中观察到IDH突变型IME中PLC的富集(图6A)。PLC的细胞组成和结构特征为:被巨噬细胞(CD68+)、B细胞(CD20+)和T细胞(CD3e+)包围的血管破裂(CD31+)(图6B和S10A )。PLC中同时存在细胞毒性T细胞(CD8 +)和辅助性T细胞(CD4+)。在CD4+和CD8+细胞群中均检测到表达GZMK、PD-1和TOX的T细胞亚群,这与混合效应样和潜在的耗竭状态相符。他们还发现滤泡辅助性T细胞(CXCL13+)和CXCR5+ B细胞之间存在关键的配体-受体相互作用(图6 C)。由于CXCL13是一种强效的B细胞趋化因子,并启动次级淋巴器官的发育,因此这种相互作用可能驱动PLC的形成。
为了在更大的队列中验证免疫热表型,他们对 51 例 IDH 突变型星形细胞瘤样本(23 例 IME 型,28 例为其他类型)进行了免疫组织化学 (IHC) 染色,共获得 306 个染色切片。相邻切片分别用 CD3(泛 T 细胞)、CD20(B 细胞)、CD8(细胞毒性 T 细胞)、CD4(辅助性 T 细胞)、CD38(浆细胞)和 CD138(浆细胞)进行染色,并在 3125 个手动标注的感兴趣区域 (ROI) 中进行定量分析(图6D)。代表性图像显示,IME 型星形细胞瘤的免疫细胞浸润明显高于非 IME 型星形细胞瘤(图 6E)。定量分析显示,IME 肿瘤中 CD3+、CD8+、CD4+和 CD20+的密度较高,为 IME 中的免疫热 TME 提供了强有力的、独立的组织学验证。
为了研究 T 细胞的空间组织,根据与 PLC 和肿瘤细胞的距离,将 CODEX 区域划分为 PLC 近区、中间区和肿瘤近区。细胞毒性 T 细胞(CD8+)密度随与 PLC 距离的增加而增加(图6F)。为了进一步解析 IME 中肿瘤浸润 T 细胞的多样性,他们从 21 个 IDH 突变型星形细胞瘤的单细胞 RNA-seq 数据中提取了所有 T 细胞,并进行了高分辨率聚类,从而鉴定出九个亚群:CD8+耗竭 T 细胞 (CD8.Tex)、组织驻留记忆 T 细胞 (CD8.Trm)、效应记忆 T 细胞 (CD8.Tem)、NK 样 T 细胞 (CD8.NK-like)、CD4+幼稚 T 细胞 (CD4.Tn)、中央记忆 T 细胞 (CD4.Tcm)、效应记忆 T 细胞 (CD4.Tem)、调节性 T 细胞 (CD4.Treg) 和 ISG+T 细胞 (CD4.ISG+)(图 6 G)。有趣的是,IME 肿瘤中 CD8.Tem 富集,而 CD8.NK-like 耗竭。值得注意的是,IME 中 CD8.Tex 水平更高(图6H)。
为了进一步评估T细胞的功能状态,他们使用已建立的特征谱分析了每个细胞的初始T细胞、效应T细胞和耗竭T细胞评分。浸润IME的T细胞的耗竭评分显著高于其他亚型(图6I)。为了在更大的队列中验证耗竭T细胞状态的富集,他们计算了基于单细胞特征谱的批量基因集变异分析(GSVA)耗竭评分。在CGGA和TCGA中,IME的耗竭评分均高于其他亚型(图6J)。这些结果表明IDHm-IME胶质瘤中存在增强的T细胞耗竭程序,提示免疫检查点阻断疗法可能对该亚组患者有益。

图6. IDHm -IME胶质瘤中的空间淋巴细胞浸润。
(A) IME 与其他 IDH 突变型星形细胞瘤患者之间血管周围淋巴细胞袖套状(PLC) 数量的比较。(B) IDHm-IME 胶质瘤中 PLC 的代表性 H&E 和 CODEX 图像。(C) 代表性 CODEX 图像显示PLC 近区域内CXCL13+ T 细胞和 CXCR5+B 细胞之间的关键配体-受体相互作用。(D) 用于独立验证的免疫组织化学 (IHC) 工作流程概述。(E) IHC染色。(F) 条形图显示不同空间区域内细胞毒性T细胞(CD8+)和辅助性T细胞(CD4+)的百分比。(G) 21例IDH突变型星形细胞瘤T细胞的UMAP。(H) 21例IDH突变型星形细胞瘤T细胞的UMAP。(I) 脊线图(左)和累积分布函数(右)显示 IDHm-IME 胶质瘤与所有其他 IDH 突变型星形细胞瘤之间的衰竭状态评分分布。(J) CGGA 和 TCGA 队列中 IME 与其他 IDH 突变型星形细胞瘤的 T 细胞耗竭评分。
07
IDHm-IME胶质瘤预后不良相关的分子特征
鉴于免疫热点IDH突变型IME胶质瘤预后较差这一悖论,他们研究了可能导致这一结果的分子特征。虽然免疫热点肿瘤通常与良好的生存率相关,但最近在IDH野生型胶质母细胞瘤中的研究表明,浸润性浆细胞通过肿瘤结合IgG促进胶质瘤干细胞的维持,并与较差的生存率相关。受此启发,他们研究了类似的机制是否也导致IME预后不良。多组学分析显示,在三个独立的数据集中,IME中免疫球蛋白成分(IGHG1/2/3和IGKC)及其相关介质(FCGR2A、CCL2和CCR2)均显著上调(图7A)。scRNA-seq数据证实了浆细胞在IME样本中的特异性富集(图7B)。CD38 和 CD138 的免疫组化染色证实,IME 中浆细胞的丰度高于其他组(图7C)。此外,采用 Ripley's Cross L 功能进行多重免疫组化染色显示,浆细胞与 IDH1-R132H+肿瘤细胞存在显著的空间共定位,表明二者之间可能存在细胞相互作用(图 7D)。
鉴于IDHm-IME中PLC结构频繁出现,他们假设血脑屏障(BBB)破坏促进免疫细胞浸润。支持这一假设的是,参与反应性星形胶质细胞介导的BBB破坏的GBP1/2和SERPINA3在IME中持续上调(图7A)。基于患者水平共表达的GBP1特征富集分析显示,GBP1与干扰素反应、IL6/JAK/STAT3信号通路和MYC靶点密切相关。为了验证GBP1的功能,他们获得了IDH突变型星形细胞瘤细胞系(TB096),证实了IDH1-R132H突变,并过表达了GBP1。体外实验表明,GBP1过表达可促进细胞增殖和迁移(图7E-F)。CGGA队列中的基因集富集分析(GSEA)将高GBP1表达与增殖(G2M检查点、E2F靶点)和迁移(EMT)通路的上调联系起来(图7 G),表明GBP1在恶性肿瘤中具有肿瘤内在作用。
这些数据共同提示了一种模型,即肿瘤内在因素和微环境因素共同导致IDHm-IME预后不良(图7H)。反应性星形胶质细胞样GD肿瘤细胞中GBP1/2和SERPINA3的上调可能促进BBB破坏,从而增加包括浆细胞在内的免疫细胞浸润。
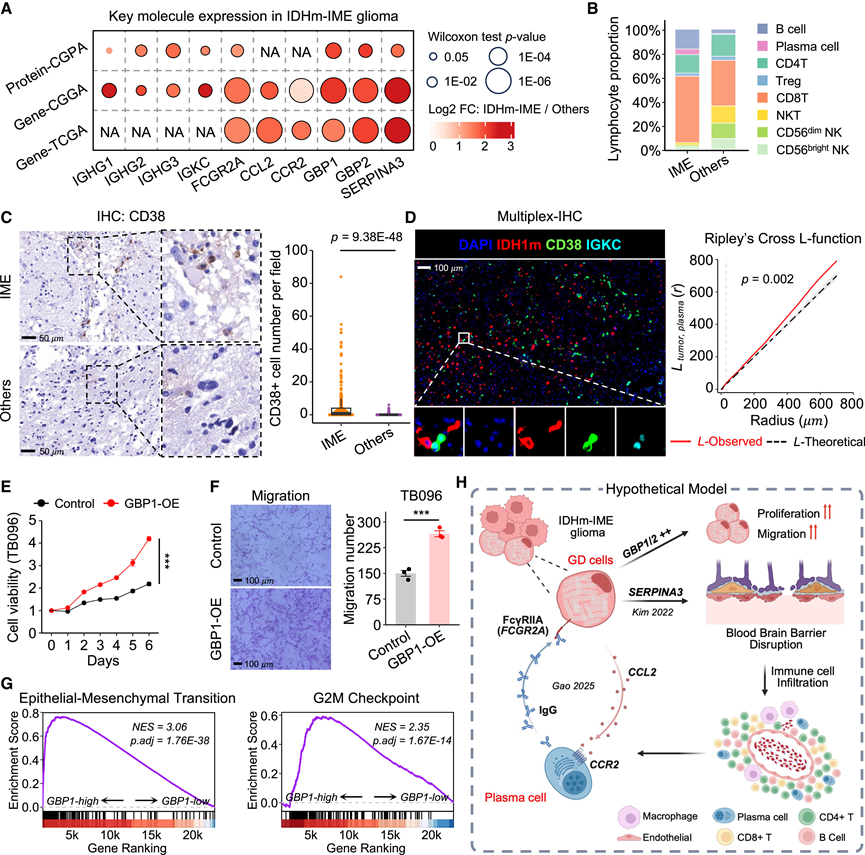
图7. IDHm-IME胶质瘤预后不良相关的分子机制。
(A) 点图显示在三个数据集(蛋白质-CGPA、基因-CGGA 和基因-TCGA)中,IDHm-IME 胶质瘤中免疫相关基因和蛋白质持续上调。(B) 堆积条形图显示 IDHm-IME 胶质瘤与其他 IDH 突变型星形细胞瘤相比淋巴细胞亚型的相对组成。(C) 代表性免疫组化图像显示IME中CD38+浆细胞浸润增加。(D) 代表性多重免疫组织化学 (mIHC) 染色图像显示IME 中IDH 突变型胶质瘤细胞 (IDH1m+) 周围浆细胞 (CD38+IGKC+)的浸润。(E) 使用细胞计数试剂盒-8 (CCK8) 检测过表达 GBP1 的 TB096 胶质瘤细胞的相对增殖情况。(F) 过表达 GBP1 的 TB096 细胞的 Transwell 迁移结果。(G) 基因集富集分析 (GSEA) 图显示CGGA 队列 ( n = 273)中 IDH 突变型星形细胞瘤患者中与GBP1高表达相关的通路。(H) 示意图总结了GBP和其他共表达的免疫相关分子导致免疫细胞浸润和不良预后的机制。
08
人工智能驱动的多组学诊断工具用于IDHm-IME胶质瘤
鉴于IDHm-IME胶质瘤独特的分子和组织病理学特征及其一致的预后影响,准确识别对于精准医疗至关重要。考虑到DNA甲基化谱分析正逐渐成为一种先进的、数据驱动的诊断准确率提升方法,他们通过将MolecularNeuroPathology (MNP) DNA甲基化分类器应用于他们匹配的DNA甲基化数据,评估基于蛋白质定义的聚类的相关性。使用MNP参考样本的无监督t -SNE分析揭示了一种独特的甲基化谱,该谱将IDHm-IME肿瘤与其他IDH突变型星形细胞瘤区分开来(图8A)。在发现队列中,对前3000个可变CpG位点的可视化显示,在基于蛋白质定义的聚类中存在一致的表观遗传差异(图8B),这促使将甲基化数据整合到诊断开发中。
因此,他们开发了一种基于人工智能的多组学诊断工具——GUIDE(图8C),用于检测IDHm-IME胶质瘤。GUIDE整合了多种组学数据,以提高诊断准确性并辅助临床决策。它包含针对图像组学、蛋白质组学、转录组学和DNA甲基化的定制分类器,并通过软投票法整合输出结果。GUIDE能够利用任何可用的组学数据,即使存在缺失的数据类型,也能快速、定量地检测IDHm-IME。
GUIDE 通过留一交叉验证法在多种组学场景下均实现了较高的平衡准确率和 F1 分数(图8D-E)。单独使用影像数据可获得约 0.84 的平衡准确率,而与转录组或 DNA 甲基化数据结合使用时,准确率显著提高。临床上,影像数据是最经济有效的输入,而 GUIDE 可灵活地通过其他组学数据提升准确率。为了进行外部验证,他们将 GUIDE 应用于一个独立的华山队列,该队列仅包含蛋白质组学数据。GUIDE重现了四个蛋白质聚类,并证实了 IME 组的生存率更低。这些结果表明,GUIDE 可作为一种高效、经济的 IDHm-IME 胶质瘤诊断解决方案,并可作为利用组织病理学和分子特征进行研究的实用工具。

图8. 用于 IDHm-IME 胶质瘤的 AI 多组学诊断实用程序。
(A) 使用 DNA 甲基化数据,通过t -SNE对新收集的 IDH 突变型星形细胞瘤和分子神经病理学 (MNP) 参考队列进行无监督聚类。(B) 热图显示了四个蛋白质聚类的不同 DNA 甲基化图谱。(C) 应用 GUIDE 从可用的组学数据中检测 IDHm-IME 神经胶质瘤的示意图工作流程。(D-E) 在组学可用性场景下,GUIDE 平衡准确度和 F1 分数的条形图,采用留一法交叉验证 (LOOCV)。
+ + + + + + + + + + +
结 论
本研究分析了时空多组学数据,发现了四个亚型:脂肪生成/脂肪酸代谢型(AFM)、增殖/祖细胞型(PPR)、免疫/间质富集型(IME)和神经元型(NEU)。PPR和IME与较差的预后相关,这一结果在TCGA和一项包含273例IDH突变型星形细胞瘤的中国队列研究中得到了验证。对189例初次发作-复发病例的纵向分析显示,肿瘤亚型呈现出向PPR/IME亚型的演化转变。从机制上讲,PPR富集了CDKN2A/B缺失,而IME则以GD增强以及耗竭T细胞和浆细胞浸润为特征。空间多组学分析将GD的形态学特征与间质样(MES样)肿瘤细胞聚集体和富含淋巴细胞的微环境联系起来。IME中的MES样肿瘤细胞过度表达干扰素刺激基因,例如GBP1,这些基因能够促进细胞增殖和迁移。最后,本研究开发了一种基于人工智能的患者分层分类器。本研究阐明了IDH突变型星形细胞瘤的蛋白质聚类,并揭示了一个免疫热点亚群,这可能为治疗研发提供信息。
+ + + + +



 English
English


