文献解读|Nat Commun(15.7):多组学分析鉴定出谱系转换型 AML 中存在 KMT2A 重排的 M-MDSC 样免疫抑制表型
✦ +
+
论文ID
原名:Multi-omics analysis identifies an M-MDSC-like immunosuppressive phenotype in lineage-switched AML with KMT2A rearrangement
译名:多组学分析鉴定出谱系转换型 AML 中存在 KMT2A 重排的 M-MDSC 样免疫抑制表型
期刊:Nature Communications
影响因子:15.7
发表时间:2025.08.26
DOI号:10.1038/s41467-025-63271-y
背 景
谱系转换(LS)是指白血病病程中白血病谱系的转换,导致疾病复发和不良临床结局。LS 曾经是一种非常罕见的现象,占白血病病例的不到 1%,但现在已成为新兴的 CD19 靶向免疫疗法[如双特异性 T 细胞衔接器、blinatumomab 和嵌合抗原受体 T 细胞 (CAR-T 细胞)]背景下的一种严重并发症;在KMT2A (MLL)重排急性淋巴细胞白血病 (KMT2A-r ALL)的背景下,它尤其成问题。特别是,由于KMT2A::AFF1是KMT2A重排急性淋巴细胞白血病(ALL)中最常见的融合基因,大多数谱系转换型急性髓系白血病(LS AML)病例均由KMT2A::AFF1重排的ALL发展而来。相比之下,伴有KMT2A::AFF1融合基因的原发性AML较为罕见,这主要是因为KMT2A::AFF1更倾向于诱导B细胞前体ALL而非AML。近年来,关于LS的几篇重要论文相继发表,主要集中于其起源细胞和谱系可塑性的机制,然而,LS中可能导致免疫逃逸的特征尚未完全阐明。
实验设计
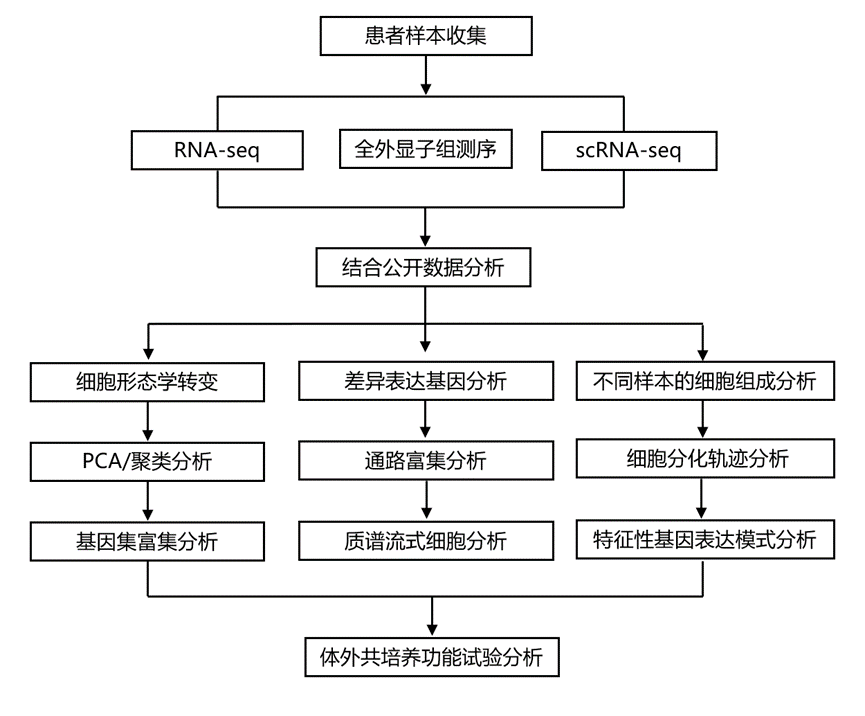
结 果
01
收集谱系转换型急性髓系白血病(AML)和对照样本,并进行数据分析
研究团队收集了5例最初表现为B细胞前体ALL后复发为LS AML的病例(图 1a),淋巴或髓系表型通过形态学和谱系特异性标志物表达进行临床诊断。所有LS AML病例均根据法美英(FAB)分型为M5型。其中4例存在KMT2A::AFF1 t(4;11)(q21;q23)重排,1例存在包含内含子7的KMT2A异常截短转录本。为避免将继发性AML误诊为LS AML,他们确认了LS发生前后 KMT2A::AFF1融合在外显子水平上相同。此外,他们收集了5例无LS的单核细胞型KMT2A重排AML病例,以下简称谱系一致(LC)AML:其中4例为初诊时即患有该疾病,1例为复发病例。LS AML1和LS AML3患者在发生LS前接受了blinatumomab治疗,LS AML3患者还接受了CD19 CAR-T细胞输注(Tisagenlecleucel)。LS AML4患者在发生LS前接受了造血干细胞移植。
他们对样本进行了转录组分析(RNA-seq)(图 1b),为了增加样本量,他们还利用了已提交的 RNA-seq 数据,从公开发表的研究中获得了 4 个数据样本,并从“治疗应用研究促进有效治疗”(TARGET)AML 项目的数据矩阵中收集了49 个数据样本(40 个初发样本,9 个复发样本)。
他们进行了主成分分析(PCA)以降低数据维度,从而更好地把握各样本间基因表达的相似性(图 1c-d)。由于该队列中的所有病例均存在KMT2A重排,且具有分化为单核细胞(M4或M5)的共同倾向,PCA图谱显示的是一个模糊的群体,而非清晰的聚类。LS AML样本倾向于彼此靠近,且具有相同聚集在一起的样本也倾向于彼此靠近。由于PCA图谱未能清晰区分LS AML,他们进行了基于RNA-seq的基因表达聚类分析,并在KMT2A重排AML群体中发现了三个共有聚类(图 1e)。通过非监督分析获得的稳定性证据验证了聚类编号,聚类1的特征是KMT2A-MLLT3和MLLT10,而聚类3主要包含ELL和MLLT4。有趣的是,所有LS AML样本都分配到聚类2。这可能反映了选择偏倚,因为大多数LS AML病例携带KMT2A::AFF1融合,而这种融合在聚类2中也很常见。
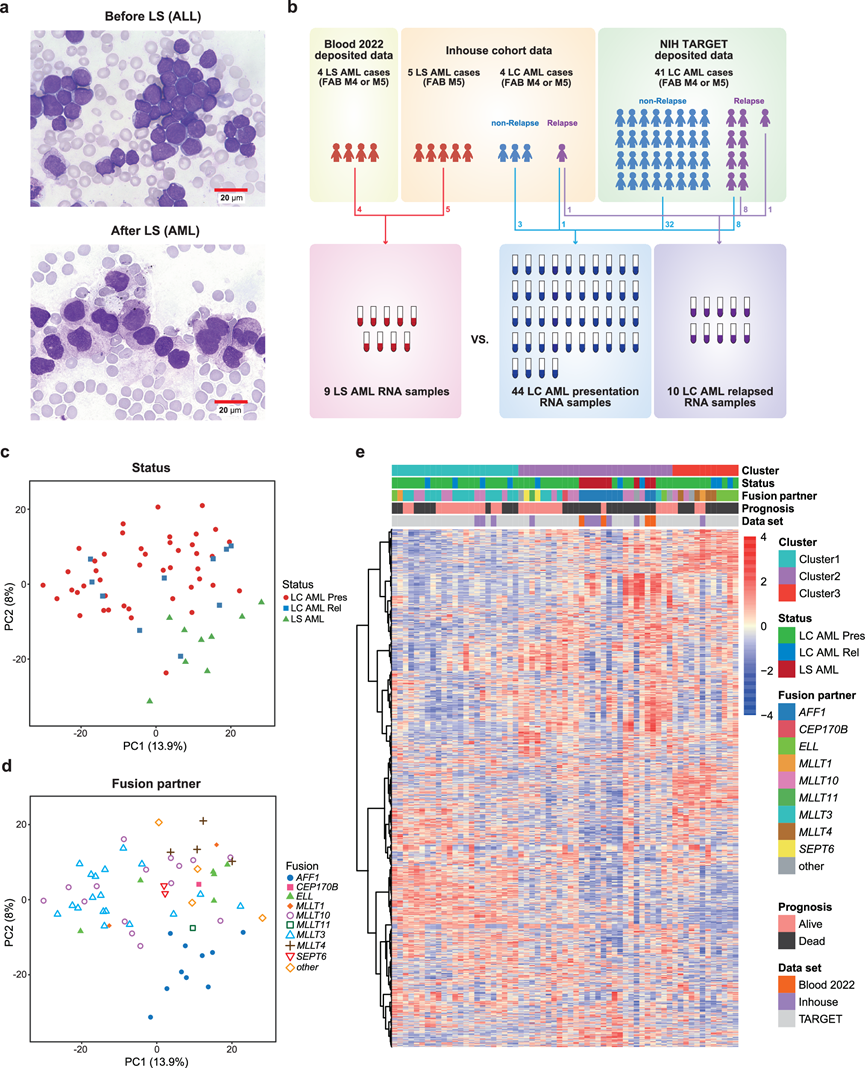
图1. 具有KMT2A重排的谱系转换 AML 的转录组学表征。
(a)形态学转换分析。(b) 实验流程图。(c-d) 每个样本的 PCA 分布图。(e) 层次聚类。
02
LS AML的特征分析
通过共识聚类分析分配到聚类2的样本(包括LS AML样本)在不同聚集在一起条件下具有更共同的转录组特征。为了鉴定LS AML和LC AML生理通路表达模式的差异,他们进行了基因集富集分析(GSEA),以比较聚类 2中的LS AML样本和LC AML样本(图 2a)。有趣的是,与适应性免疫(紫色)和抗原呈递(蓝色)相关的基因集在后15个基因集中富集。这表明,与聚类 2中的LC AML相比,LS AML的特征是获得性免疫系统受到抑制和抗原呈递能力降低,尤其是在主要组织相容性复合体(MHC)II类分子的背景下。他们还通过GSEA将LS AML样本与所有LC AML样本进行了比较。与聚类 2的比较结果相似,LS AML中与适应性免疫和抗原呈递相关的基因集显著下调。值得注意的是,在更广泛的比较中,抗原呈递相关的基因集排名更加突出。
随后,他们分析了在LS AML中观察到的与适应性免疫和抗原呈递相关的下调基因集。为了检测每个基因集组中导致低富集信号的共同基因,他们对上述两个基因集组进行了前沿分析,这两个基因集组在GSEA分析后聚类2的排名垫底(图 2b-c)。在与适应性免疫相关的基因集中,IRF4、GATA3和HLA-DRB1的下调尤为显著。在与抗原呈递相关的基因集中,MHC II类基因(包括HLA-DR [ HLA-DRA、DRB1和DRB5 ])的下调尤为显著。在单核细胞谱系分化过程中,HLA-DR的表达通常最早在粒细胞-单核细胞祖细胞阶段即可观察到。单核细胞来源的髓系抑制细胞(M-MDSC)定义为 HLA-DR 表达低或不表达的单核细胞(即 CD11b+CD14+CD15- HLA-DR-)。从这个角度来看,LS AML 样本中免疫抑制基因的表达模式以及 HLA-DR 的下调表明,LS AML 可能与 M-MDSC 相似。此外,据报道,干扰素调节因子 4 (IRF4) 的缺乏会促进髓系来源抑制细胞(MDSC)的生成并增加 M-MDSC 的扩增,这与上述假设相符。
为了验证LS AML与M-MDSC的相似性高于LC AML这一假设,他们将基因表达谱与先前报道的M-MDSC基因特征进行了比较。“M-MDSC特征细胞代表”包含在M-MDSC中与经典单核细胞相比显著上调的16个基因(ORM1、S100P、SLCO4C1、CYP1B1、CLEC4D、CHD7、CKAP4、MSRB1、CLU、CD82、CPEB4、TLK1、OSBPL8、ABHD2、ATP6V1E1和ROCK1)。当利用GSEA比较M-MDSC特征时,他们发现它在LS AML中的富集程度显著高于LC AML(图 2d)。此外,与携带KMT2A::AFF1 的LC AML 相比,携带KMT2A::AFF1 的LS AML 中 M-MDSC 特征也更加丰富,这表明其特征可能来源于 LS 而不是AFF1融合(图 2e)。
此外,他们检测了LS AML和LC AML之间的差异表达基因(DEG)(图 2f)。在M-MDSC相关基因中,VEGFA、CD82、ORM1和MSRB1在LS AML中的表达显著上调。这些结果表明,与LC AML相比,LS AML的基因表达模式更接近于M-MDSC。另外,内部的 LS AML 病例的全外显子组测序(WES)鉴定出几个突变,其中,LS AML1 和 LS AML3 中TP53的高变异等位基因频率 (VAF) 以及 LS AML2 中CDKN2A的高变异等位基因频率归因于拷贝数改变。
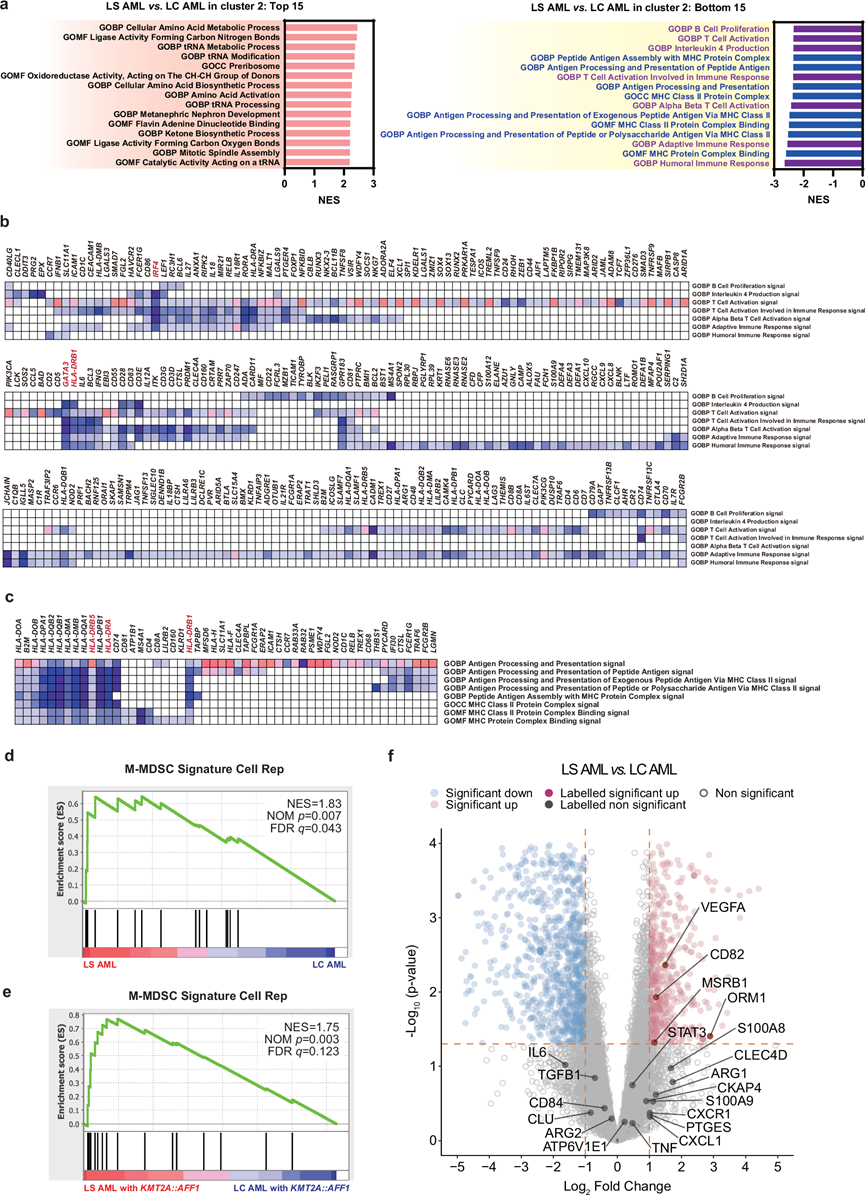
图2. 谱系转换AML中的基因集富集分析和差异表达基因分析。
(a) 通过基因集富集分析 (GSEA) 计算得出的标准化富集得分 (NES) 排名前 15 和后 15 的基因集。(b-c) 在比较 聚类2 中的 LS AML 和 LC AML 时,排名后 15 的适应性免疫相关基因集和抗原呈递相关基因集的前沿分析。(d) 比较 LS AML 和 LC AML 的M -MDSC 特征的富集分析。(e) 将 LS AML 与KMT2A::AFF1进行比较以及将 LC AML 与KMT2A::AFF1进行比较的 M-MDSC 特征的富集分析。(f) 火山图显示LS AML和LC AML之间的DEG。
03
质谱流式细胞分析
RNA-seq结果表明,LS AML样本的特征比LC AML样本更接近M-MDSC;然而,肿瘤整体RNA-seq数据可能受到分析样本中非肿瘤细胞的影响。为了验证观察到的特征是AML细胞本身还是正常(非AML来源)的M-MDSC所致,并确认MDSC特异性表面抗原在单细胞水平上的表达,他们设计了一个包含39个标记物的质谱流式细胞panel,可用于同时分析白血病细胞和免疫细胞。
首先,他们使用39个多参数对获得的质谱流式细胞技术(CyTOF)数据进行降维,然后使用基于t分布随机邻域嵌入(t-SNE)算法的可视化工具viSNE进行可视化。viSNE图清晰地将AML细胞(粉色)与其他正常免疫细胞区分开来(图 3a)。接下来,他们使用相同的数据进行常规设门,以识别具有M-MDSC表型(即CD11b+CD14+CD15- HLA-DR-)的细胞,而不区分AML细胞或其他正常细胞。使用来自健康个体的外周血单核细胞(PBMC)作为参考,其中含有2.3%的CD11b+CD14+CD15- HLA-DR-细胞。既往研究表明,健康个体PBMC中 M-MDSC 的比例约为 0.5%-3%。最后,将鉴定出的具有 M-MDSC 表型的细胞叠加到 viSNE 图(红色部分)上,以确定它们是否为 AML 细胞(图 3a)。鉴定出的具有 M-MDSC 表型的细胞大多为 AML 细胞。他们发现了LS AML1 细胞表达的 M-MDSC 相关标记物(图3b)。值得注意的是,在 LS AML 样本中,M-MDSC 样 AML 细胞占总 AML 细胞的比例显著更高(图 3c)。此外,LS AML2 患者中 M-MDSC 样 AML 细胞群在 LS 发病 70 天后(即病情加重时)增加,提示该细胞群可能参与疾病进展(图 3a)。这些结果表明,部分 AML 细胞具有 M-MDSC 样特性,且在 LS AML 中比在 LC AML 中更为常见。此外,他们评估了每位患者在 LS 发病前后白血病细胞的 HLA-DR 表达情况。所有患者的 ALL 细胞 HLA-DR 表达均 >95%,且在 LS 发病后下降;这表明 LS 发生后 HLA-DR 表达下调。
此外,在低危急性髓系白血病(LS AML)样本中,CD4+ T细胞群中调节性T细胞(Treg,CD4 +CD25+CD127- T细胞)及其效应亚群(CD4+CD25+CD127-CD45RA-Foxp3 highT细胞)的比例高于低危LC AML样本(图3d-e)。综合来看,M-MDSC 样 AML 细胞群的增加以及 CD4 +T 细胞群中 Treg 细胞数量的增加,表明 LS AML 患者体内存在免疫抑制环境。
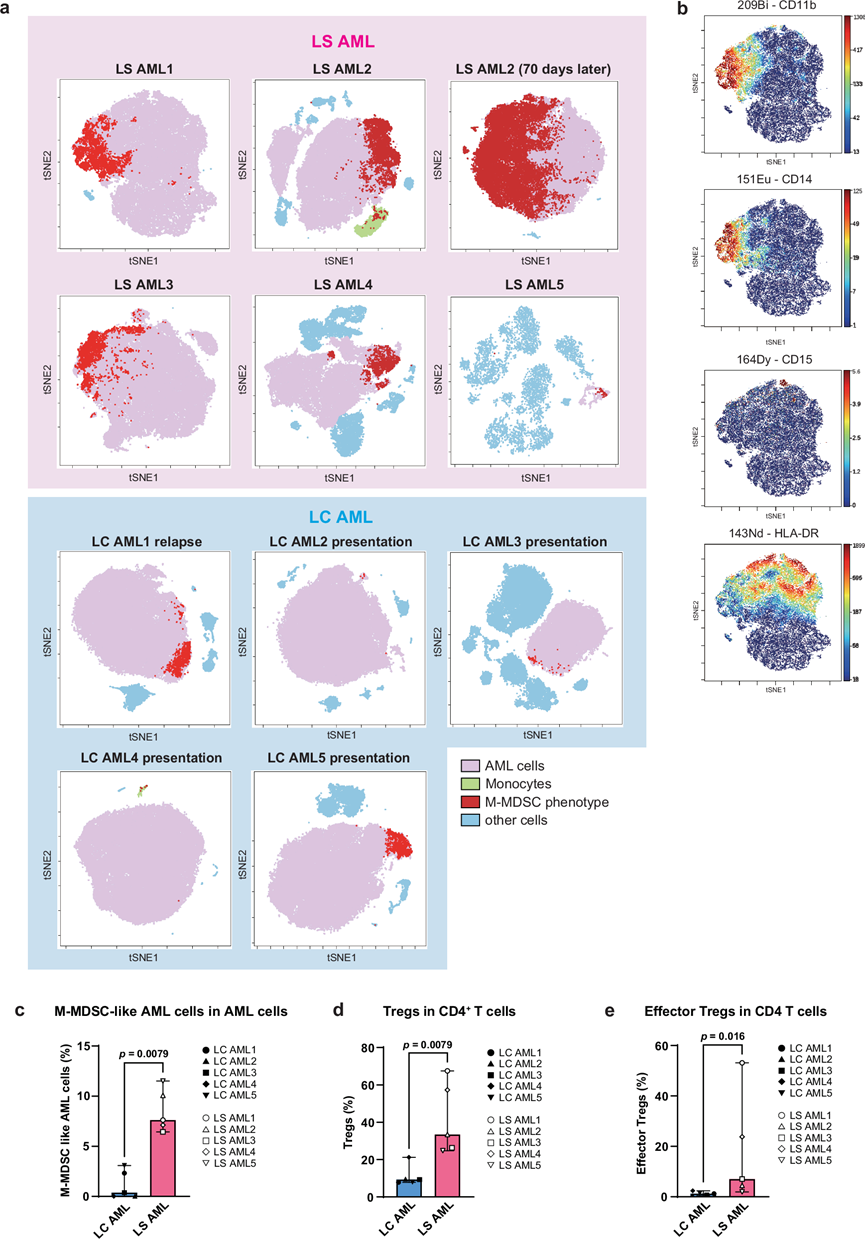
图3. 通过质谱流式细胞检测 AML 样本中的 M-MDSC 样 AML 细胞和 Treg。
(a-b) tSNE图显示 39 种标志物的表达。(c) AML 细胞群中M-MDSC 样 AML 细胞的百分比。(d) CD4+T 细胞群中 Treg(CD4+ CD25+ CD127- T 细胞)的百分比。(e) CD4+ T 细胞群中效应 Treg(CD4+ CD25+ CD127- CD45RA- Foxp3high T 细胞)的百分比。
04
免疫系统调控相关的特征性基因表达模式
之后,他们通过流式细胞分析从LS AML和LC AML样本中分选出CD45低表达的存活白血病原始细胞,然后进行单细胞转录组分析(scRNA-seq)和数据整理。随后,利用均匀流形逼近和投影(UMAP)方法对AML细胞的单细胞数据进行降维,并结合来自三名患有自身免疫性疾病(系统性红斑狼疮:SLE、系统性幼年特发性关节炎:sJIA、干燥综合征)的儿童患者的骨髓单核细胞数据进行分析(图 4a),这些自身免疫性疾病患者存在慢性炎症,这促进了MDSC的生成。正如预期的那样,具有单核细胞特征且缺乏HLA-DR表达的AML细胞富集了M-MDSC特征(图 4b)。
随后,他们根据M-MDSC特征基因的标准化表达水平将AML细胞分为“M-MDSC样”和“非M-MDSC样”两类(图4c),然后使用Metascape软件比较M-MDSC样LS AML亚群和非M-MDSC样LS AML亚群中与造血相关的基因集的富集情况。在M-MDSC样LS AML亚群中,许多与免疫相关的基因集,包括调节免疫反应、细胞因子产生和免疫效应过程的通路,均高表达(图4d)。此外,比较过程中观察到的上调和下调基因集与自身免疫性疾病患者中M-MDSC和非M-MDSC髓系细胞的比较结果相似,表明M-MDSC样LS AML细胞与M-MDSC具有免疫学相似性。为了进一步揭示M-MDSC样LS AML亚群基因集特征之间的关系,他们选取了一部分富集通路,并将其绘制成网络图;在网络图中,与更多基因相关的通路具有更显著的p值。此外,参与免疫系统调控和细胞活化的通路位于网络中心,并在图中形成了一个密集的网络(图 4e)。该通路富集网络强调了M-MDSC样AML亚群与免疫系统的关联性及其在免疫系统调控中的作用。
为了评估LS AML细胞与自身免疫性疾病患者体内M-MDSC之间的同源性,他们使用SPRING流程进行了分化轨迹分析。所得图谱揭示了可能的分化轨迹,其中包括一条描绘细胞从造血干细胞(HSC)/多能祖细胞(MPP)发育为M-MDSC的连续谱(图 4f)。在轨迹图中,自身免疫性疾病患者的M-MDSC位于右上角,并具有富集的M-MDSC特征信号。有趣的是,尽管LS AML细胞与M-MDSC位于相似的轨迹上(图谱右下角),但它们与M-MDSC所在区域的重叠并不多。这两个群体分离的可能原因是 M-MDSC 样 LS AML 细胞表达中性粒细胞-髓系祖细胞特征,而 M-MDSC 中未观察到这种特征。
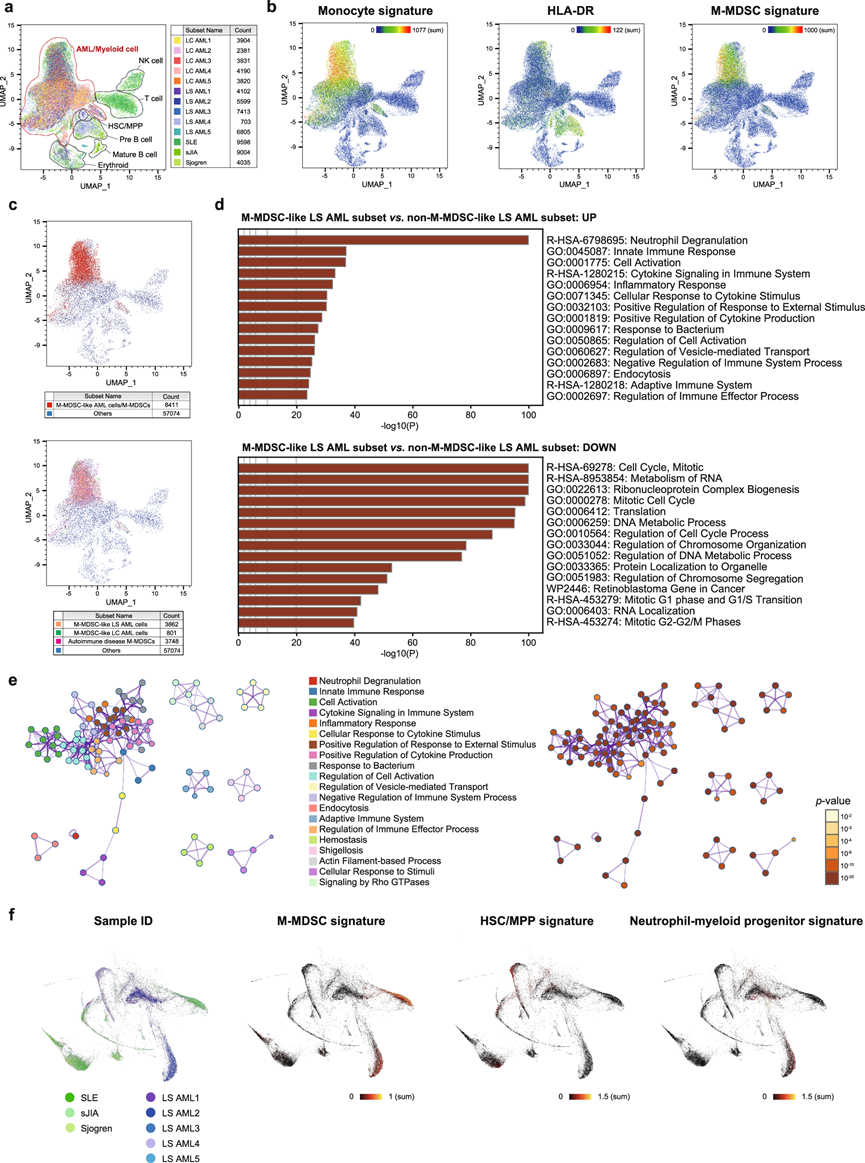
图4 谱系转换 AML 与自身免疫性疾病中的 M-MDSC 的scRNA-seq。
(a) 从五个 LS AML、五个 LC AML 和三个自身免疫性疾病样本中获得的单细胞转录组数据的 UMAP 图。(b) UMAP上基因特征(单核细胞、HLA-DR 和 M-MDSC)的标准化强度用颜色表示。(c) M -MDSC 样 AML 亚群和 M-MDSC(红色)定义为 M-MDSC 特征基因标准化表达水平≥150 的细胞(上图)。在该亚群中,LS AML 细胞显示为橙色,LC AML 细胞显示为绿色,自身免疫性疾病 M-MDSC 显示为红色(下图)。(d) 通过造血基因集分析比较了 M-MDSC 样 LS AML 亚群和非 M-MDSC 样 LS AML 亚群。(e) 富含 M-MDSC 样 LS AML 子集特征基因集的网络。(f) 由 SPRING 流程创建的k最近邻图。
05
谱系转换的AML细胞在体外实验中抑制T细胞增殖并诱导Treg细胞
功能评估对于确认MDSC的存在至关重要。接下来,他们探究了LS AML细胞是否具有与MDSC相同的免疫抑制特性,包括T细胞抑制和Treg增强。
首先,他们进行了T细胞抑制实验。使用FACSAria II流式细胞仪(BD)从健康供体PBMC中分选出应答性CD4+CD25- CD45RA+ T细胞(幼稚Tconv)(纯度>95%),用羧基荧光素琥珀酰亚胺酯(CFSE)染色,然后在IL-2和CD3/CD28磁珠存在下与不同数量的AML细胞共培养。作为T细胞抑制的阳性对照,他们在添加了IL-6、GM-CSF和异丙肾上腺素的培养基中培养健康供体PBMC ,诱导产生M-MDSC。共培养后,计数分裂的T细胞数量,并在第五天通过细胞内染色检测T细胞产生的干扰素-γ(IFN-γ)(图 5a)。正如预期,LS AML细胞以剂量依赖的方式抑制T细胞增殖,且抑制程度远高于LC AML细胞(图 5b-c)。此外,与LC AML细胞的情况相反,随着LS AML细胞比例的增加,T细胞产生的IFN-γ量减少(图 5b-d)。这些数据表明,LS AML细胞以剂量依赖的方式抑制T细胞产生IFN-γ。当将幼稚Tconv细胞与诱导的M-MDSC细胞共培养时,获得了相同的结果(图 5c-d)。
之后,他们探究了LS AML细胞是否能增加Treg细胞的数量。通过磁珠分选从健康个体中分离出的CD4+ T细胞与AML细胞或诱导的M-MDSC(比例为1:1)共培养5天。然后,计算CD4+T细胞群中Treg细胞和效应Treg细胞的百分比(图 5e)。用于定义Treg细胞(CD4+CD25+CD127- T细胞)和效应Treg细胞(CD4+CD25+CD127-CD45RA-Foxp3 high T细胞;第二组分)的设门策略基于从健康对照PBMC中分离出的CD4+ T细胞(图 5f)。值得注意的是,与LS AML细胞共培养可显著增加效应Treg细胞的比例,与诱导的M-MDSC细胞共培养亦是如此,且二者均优于与LC AML细胞共培养(图 5g)。综上所述,这些数据表明LS AML细胞能够抑制T细胞增殖并增加效应Treg细胞的比例,提示其具有与MDSC细胞类似的免疫抑制特性。
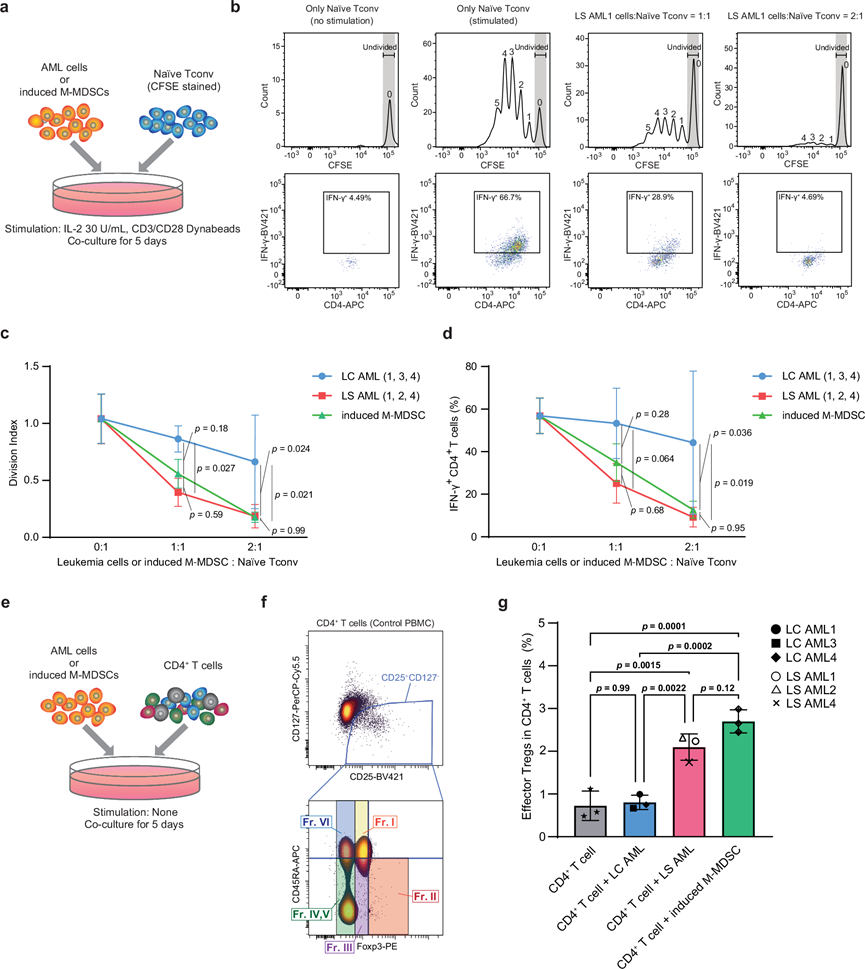
图5. 功能性体外共培养试验验证了谱系转换 AML 的 MDSC 样特征。
(a) 使用 AML 细胞和诱导的 M-MDSC 进行 T 细胞抑制试验的示意图。(b) IFN-γ 细胞内染色的代表性 CFSE 直方图和点图。(c) 不同[AML 细胞或诱导的 M-MDSC]/T 细胞比例下的 T 细胞分裂指数。(d) 不同 [AML 细胞或诱导的 M-MDSC]/T 细胞比率下总 CD4+ T 细胞群中 IFN-γ+CD4+ T 细胞的百分比。(e) Treg 共培养试验示意图。(f) 用于识别对照 PBMC中CD4+ T 细胞内效应 Treg 的门控标准。(g) 共培养 5 天后CD4+ T 细胞群中效应 Treg 的百分比。
+ + + + + + + + + + +
结 论
本研究对AML患者样本进行了多组学分析,发现具有KMT2A -r的LS AML细胞具有M-MDSC样特征。单细胞质谱流式细胞分析显示,与谱系一致的KMT2A- r AML相比,LS AML中M-MDSC样细胞数量增加;单细胞转录组学分析鉴定出该细胞群中免疫调节基因的独特表达模式。此外,体外实验证实LS AML细胞具有抑制T细胞的免疫抑制能力,与MDSC类似。这些数据有助于深入了解 LS AML 复杂发病机制的免疫学方面,以及未来治疗方法的开发。
+ + + + +



 English
English


