文献解读|Clin Cancer Res(10.2):同步性子宫内膜样癌和卵巢癌的蛋白质组学研究
✦ +
+
论文ID
原名:A Proteogenomic View of Synchronous Endometrioid Endometrial and Ovarian Cancer
译名:同步性子宫内膜样癌和卵巢癌的蛋白质组学研究
期刊:Clinical Cancer Research
影响因子:10.2
发表时间:2025.12.03
DOI号:10.1158/1078-0432.CCR-24-1763
背 景
越来越多的基因组学证据表明,同步性子宫内膜癌和卵巢癌(SEOC)代表了克隆相关的原发性和转移性肿瘤。此前缺乏对SEOC整体蛋白质图谱的系统性分析,而对SEOC整体蛋白质图谱的系统性分析有望揭示已知基因改变的功能和疾病特异性后果、转移方向以及用于区分SEOC和单发肿瘤的准确组织学标志物。
实验设计
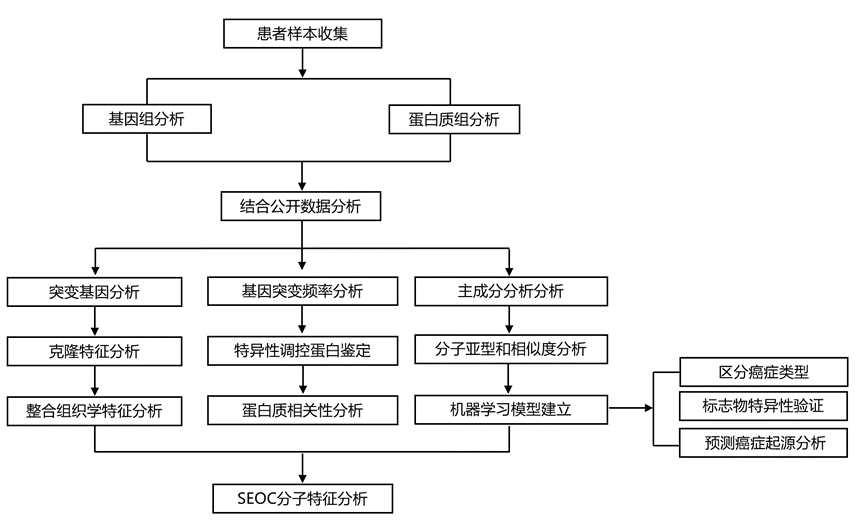
结 果
01
SEOC的蛋白质组学分析
研究团队对三组患者(共64例)进行了系统的蛋白质组学分析,这些患者术后均诊断为子宫内膜样肿瘤,肿瘤组织学检查结果显示其位于卵巢、子宫或卵巢和子宫(图1A)。单部位子宫内膜样卵巢癌(EOC)组包含9例患者,单部位子宫内膜样癌(EEC)组包含26例患者。第三组包含29例同时患有子宫和卵巢癌(SEOC)的患者,即子宫和卵巢均存在子宫内膜样肿瘤。所有患者均在三家国际妇科肿瘤中心(芝加哥、温哥华、图宾根)接受治疗(图1A-B)。
研究团队首先分析了SEOC的基因组数据,结果显示错义突变是最主要的突变类型(>90%),其次是无义突变和剪接位点突变。C>T单核苷酸变异(SNV)是最常见的SNV类型。先前报道在卵巢癌中发生突变的已知驱动基因,例如PTEN、PI3KCA和ARID1A,均位列前十位突变基因之列(图1C)。与既往研究一致,27例卵巢癌中有25例具有克隆相关性,且不同癌位点间共有核心突变的数量差异很大(图1D-E)。他们再次确认了8例SEOC的克隆关系,但他们未能确认两例温哥华病例(VAN_04和VAN_22)的克隆关系。这可能部分归因于本研究使用了来自潜在异质性肿瘤的两个独立样本,这些肿瘤的突变负荷各不相同,以及基因组的差异。
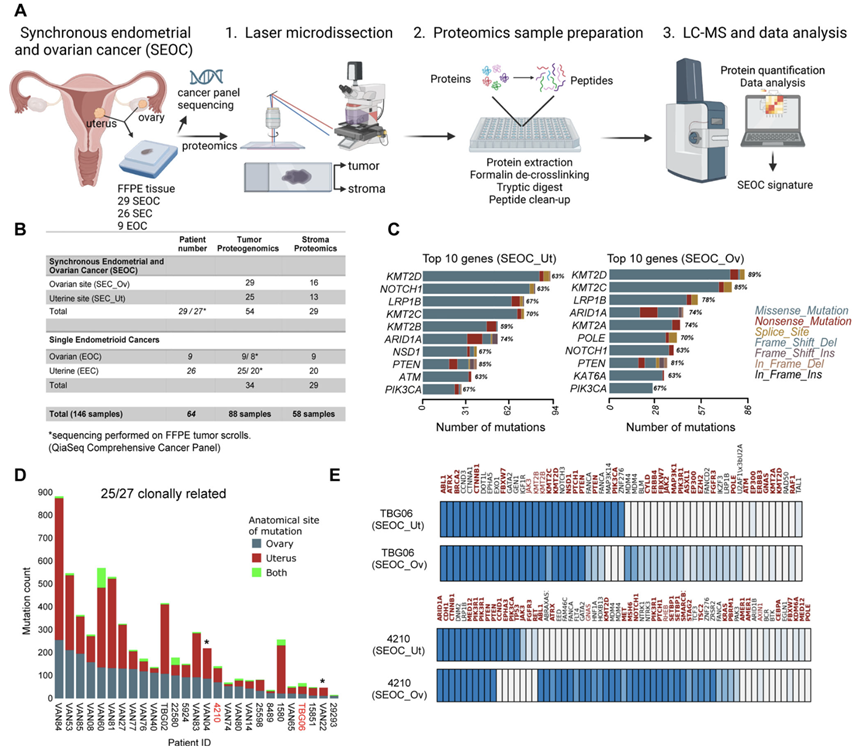
图1. 蛋白质基因组学阐明了同步癌症的分子图谱。
(A) 研究设计。(B) 用于蛋白质组学分析的患者数量和组织部位。(C) 在子宫和卵巢中发现的前十个SEOC突变基因。(D) 在SEOC的子宫和卵巢解剖部位中发现的共有突变和特有突变。(E) 对两名SEOC患者的子宫和卵巢癌部位进行比较。
02
SEOC在基因上与发生在子宫或卵巢的单个子宫内膜样癌不同
除了SEOC病例外,本研究还纳入EOC和EEC患者样本(图2A)。染色质重塑和转录因子相关基因,包括KMT基因家族、EP300、ARID1A和KAT6A,以及CTNNB1(β-catenin)、LRP1B、NOTCH2和PIK3CA,在所有三组患者中均发生突变,这表明子宫内膜样组织学具有共同的遗传驱动因素,且与解剖部位无关(图1C和图2B)。与TCGA泛癌研究的比较显示,整个队列中突变最显著的基因与子宫内膜样癌的基因谱重叠程度远高于与非子宫内膜样组织学类型的上皮性卵巢癌的重叠程度(图2C)。在SEOC中发现的突变特征与EEC相似,但与EOC不同(图2D)。这在疾病驱动基因PTEN和ARID1A以及许多其他癌症相关基因(例如CREBBP、NOTCH2、ERBB4)中尤为明显(图2D-E)。他们研究了三种样本在共有突变的等位基因频率上是否存在差异,这可能提示转移的方向性。子宫内膜肿瘤的平均比值为 0.43(标准差 = 0.32),卵巢肿瘤的平均比值为 0.51(标准差 = 0.28),两者差异有统计学意义,这支持了SEOC可能起源于子宫内膜并从子宫内膜(亚克隆)进展到卵巢(克隆)的观点。
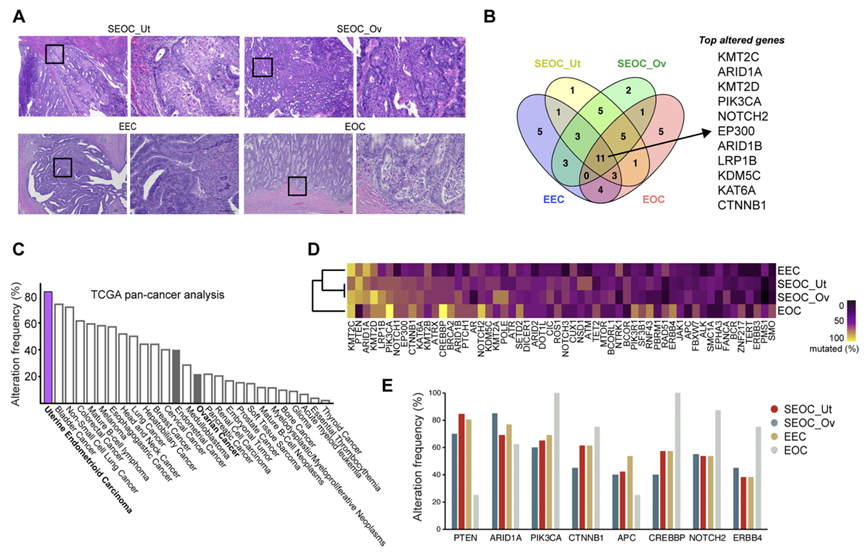
图2. 同步发生的癌症与子宫内膜样组织学的单个子宫癌具有相似的突变特征。
(A) 代表性的子宫和卵巢双发(患者匹配部位)及单发子宫内膜样癌组织H&E染色切片。(B) 按部位划分的子宫双发及单发子宫内膜样癌和单发卵巢内膜样癌共有或特有的前30个突变基因。(C) 对子宫和卵巢双发及单发子宫内膜样癌共有基因进行TCGA泛癌突变比较。(D) 基于突变频率对前30个突变基因进行无监督层次聚类分析。(E) 按双发及单发子宫内膜样癌部位划分的选定基因的突变频率。
03
SEOC具有独特的基质蛋白质
基因组分析表明,SEOC 具有克隆相关性,且与单个 EEC 的相似性高于单个 EOC。为了全面表征 SEOC,他们对来自 64 例患者的 146 个样本进行了激光显微切割,随后进行基于质谱的蛋白质组学分析,以区分肿瘤和间质成分(图1A)。样本在离子阱迁移质谱仪上进行分析,并采用无标记蛋白质组定量方法,最终得到 88 个肿瘤样本和 56 个间质样本。他们定量分析了每个肿瘤样本的中位数为 6378 个蛋白质,每个间质样本的中位数为5400个蛋白质,且各组间蛋白质水平的变异性相似。这些蛋白质表现出很强的区室特异性,各样本组中上皮和间质标志物均显著富集(图3A-C),而样本采集地点(温哥华、图宾根和芝加哥)对差异表达蛋白(DEP)的数量影响甚微(图3D)。总体而言,同一患者内两种癌症(子宫癌与卵巢癌)的蛋白质相关性高于不同患者间两种或单一癌症的蛋白质相关性(图3E)。切除肿瘤的解剖部位是蛋白质组的一个重要混杂因素,在间质中更为显著(图3D)。尽管如此,所有单一部位和SEOC的比较分别在肿瘤和间质区室中鉴定出400个和335个特异性调控蛋白(图3D-F)。
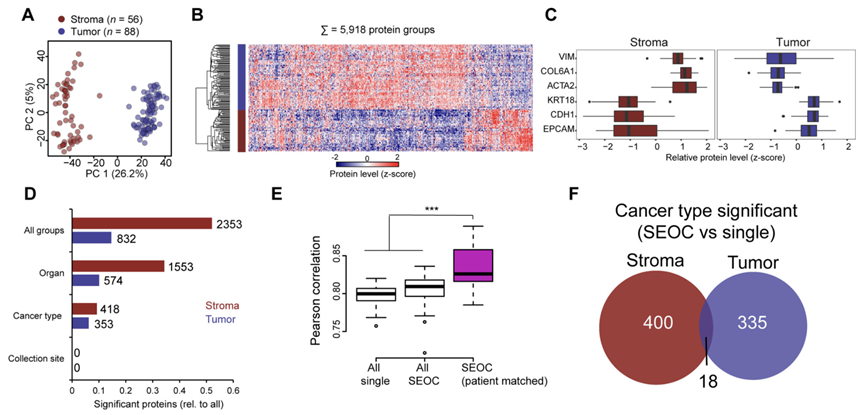
图3. 单发子宫癌和卵巢癌以及同步子宫癌和卵巢癌的基质和肿瘤的蛋白质组学分析。
(A) 对所有肿瘤(n=88)和间质(n=56)蛋白质组进行主成分分析。(B) 热图显示了基于5918个独特蛋白质对所有肿瘤和间质样本进行的无监督层次聚类。(C) 与图B相关的典型间质和肿瘤标志物的相对蛋白质水平(z分数)的箱线图。(D) 基于所有组(EEC、EOC、SEOC_Ut、EOC_Ov)、器官部位(子宫与卵巢)、癌症类型(单癌与双癌)和采集地点(温哥华、图宾根、芝加哥)的显著变化蛋白质数量。(E) 同步癌(患者匹配比较)或双癌(所有患者)与单癌(所有患者)之间的蛋白质相关性。(F) 维恩图显示了肿瘤和基质来源的显著蛋白质(<10%)之间的重叠情况。
04
子宫相关的特征分析
与单一癌相比,在SEOC的肿瘤和间质区室中鉴定出显著表达的蛋白质,这促使他们进一步研究这些特征。间质蛋白质组数据在区分双癌和单一癌方面比肿瘤蛋白质组表现得更好,尤其是在考虑器官相关蛋白质组差异时(图4 -D)。与基因组分析类似,接下来他们探究SEOC肿瘤蛋白质组与单一子宫内膜癌(EEC)还是单一卵巢癌(EOC)更相似,以揭示其可能的起源部位。首先纳入了来自人类蛋白质图谱(Human Protein Atlas)组织富集谱的健康子宫和卵巢蛋白质组特征(包含47种蛋白质),其次,采用一种无偏方法筛选出表达变异最大的1000种蛋白质。两种方法的结果均表明,SEOC的平均肿瘤蛋白质组与EEC的聚类比与单一EOC的聚类更接近(图4E)。综合来看,基因组(图 2)和蛋白质组数据表明,平均而言,同步癌与单个子宫癌更为相似,这表明大多数低级别同步肿瘤起源于子宫。
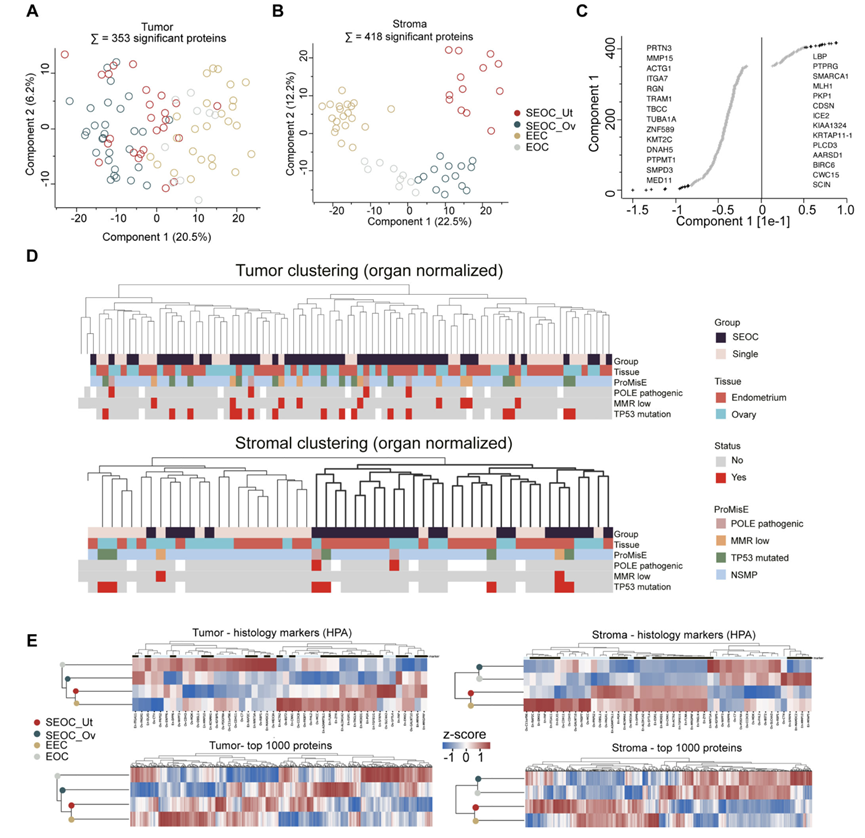
图4. 单发子宫癌和卵巢癌以及同步子宫癌和卵巢癌的基质和肿瘤的蛋白质组学分析。
(A) 353 种癌症类型(单癌或双癌)特异性肿瘤蛋白的主成分分析 (PCA)。(B) 418 种癌症类型(单癌或双癌)特异性基质蛋白的 PCA。(C) 基质 PCA 的蛋白载荷。(D) 上:对肿瘤样本进行无监督层次聚类。下:基质样本的相应分析。(E) 基于人类蛋白质图谱 (HPA) 的富集谱(上图)或数据集中 1000 个表达变异最大的蛋白质(下图),使用基于 47 个组织学标记的组平均蛋白质组的无监督层次聚类进行热图分析。
05
蛋白质组学预测因子
目前用于诊断SEOC的组织病理学标准并不十分严格。然而,将其与单纯性卵巢上皮EEC或EOC区分开来具有重要的临床意义,因为SEOC患者的预后通常较好,且通常仅需手术治疗,无需辅助治疗。因此,他们利用已获得的区室解析定量蛋白质组数据,对用于区分SEOC和单纯性癌症的蛋白质进行优先级排序。基于在所有三个组中定量的6000多个独特蛋白质,采用机器学习(ML)方法进行了特征重要性分析。将归一化的蛋白质测量值进行特征重要性分析,该分析基于开源工具OmicLearn中的ExtraTrees方法进行特征选择,并采用AdaBoost机器学习算法。在此,将数据分为训练集(80%)和测试集(20%),并进行了五轮交叉验证(图5A)。受试者工作特征(ROC)曲线显示出较高的曲线下面积(AUC)值(间质为0.92,肿瘤为0.88),能够清晰地区分不同的癌症类型(图5B-E)。与同步癌相比,间质中主要过表达的蛋白特征包括CFAP20、TMEM115、AKTIP、GALNT3和ARAP1(图5C)。肿瘤中排名靠前的蛋白特征包括EPRS、PIGS、AKR1B1、FAM3C、ATP13A1和COMMD1(图5E)。
值得注意的是,排名靠前的特征蛋白的差异倍数幅度较小至中等,这凸显了基于定量质谱的蛋白质组学在识别疾病分子标志物方面的强大能力。由于目前尚无其他蛋白质组学数据可用于进一步验证这些发现,他们分析了TCGA泛癌研究以验证标志物的特异性。由于大多数排名靠前的肿瘤蛋白在单一癌症中均过表达,他们推测这些标志物在TCGA子宫内膜样癌研究中也会过表达。事实上,与其他所有癌症类型相比,子宫内膜样癌和子宫内膜癌的mRNA上调程度最高,远高于卵巢癌,这清楚地反映了其对子宫组织学的特异性。
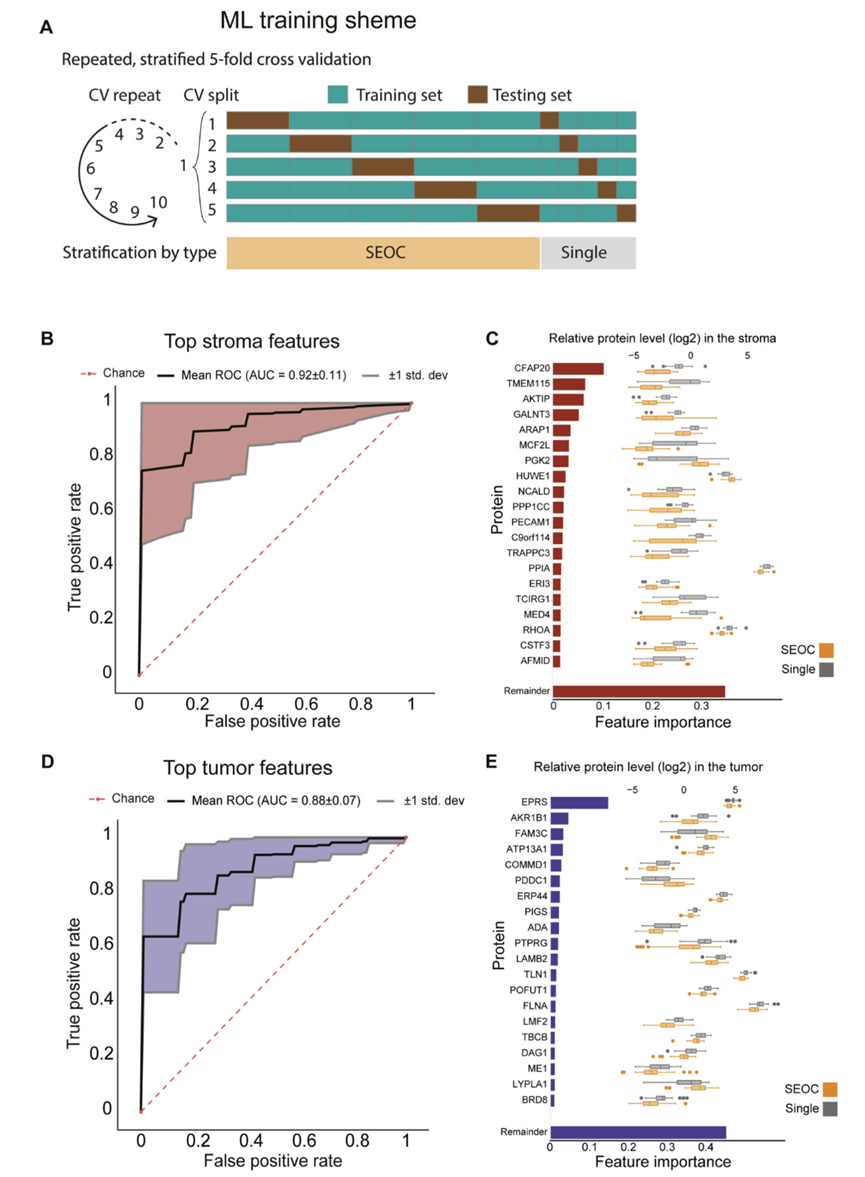
图5. 机器学习可以利用蛋白质组学数据预测同步癌症的起源。
(A) 基于机器学习的分层策略概述。(B) 基于基质区室中20个最具特征蛋白的SEOC预测器的受试者工作特征曲线(ROC曲线)。(C) 区分双重癌和单一癌的前20个基质特异性候选蛋白的相对蛋白定量值。(D) 基于肿瘤区室中20个最具特征蛋白的SEOC预测器的ROC曲线。(E) 区分双重癌和单一癌的前20个肿瘤特异性候选蛋白的相对蛋白定量值。
+ + + + + + + + + + +
结 论
本研究对来自三家国际妇科肿瘤治疗中心(芝加哥、温哥华和图宾根)的29例确诊为SEOC的患者进行了系统的蛋白质组学分析。为了与单发肿瘤进行直接比较,纳入了9例单发子宫内膜样卵巢癌患者和26例单发子宫内膜样癌患者。对于所有64例患者,进行了包含275个基因的癌症基因组测序,并结合蛋白质组学分析,对连续组织切片进行分析,以比较整体蛋白质组(6000多种蛋白质)、肿瘤蛋白质组和间质蛋白质组数据,大多数SEOC具有克隆相关性。蛋白质组分析揭示了SEOC与单个肿瘤之间的显著差异,并强调了基质蛋白质组在定义和识别SEOC中的重要性。本研究鉴定了分子特征独特的SEOC基质蛋白质,这些蛋白质与EEC的相关性更高。
+ + + + +



 English
English


